联系我们
- 电话/微信:18520902353
- 客服QQ:3597831168
- 邮箱:info@wemaxnano.com
- 地址:广东省佛山市南海区狮山镇长兴西路12号建发风梅岭产业园9号楼
一、研究背景
由脱细胞细胞外基质(dECM)组成的组织工程支架在许多应用中都显示出支持再生的巨大能力。脱细胞细胞外基质由纤维蛋白、蛋白多糖、生长因子、细胞因子和 mRNA 组成,可提供结构和生物线索,从而引导组织重塑。细胞与 dECM 相互作用并吸收 dECM,从而释放出生物活性产物,如趋化性低分子量蛋白、血管生成生长因子和 mRNA。组织特异性 dECM 通过支持细胞招募、增殖和组织特异性分化,成功促进了血管生成、肌生成、神经原生成和免疫调节行为。小肠粘膜下层(SIS)是市场上最著名的 dECM 支架之一,因为它含有支持肠粘膜持续再生所需的大量生长因子和营养物质。在临床试验中,SIS 支架已在气道、腹壁、横膈膜、肠道、膀胱、肩袖、皮肤和尿道组织的再生方面取得了成功。
将 dECM 制成用于目标应用的特殊结构仍具有挑战性。蛋白质和生长因子的生物活性很容易在酶消化、加热或刺激性溶剂的作用下失活。目前,临床实践仅限于使用原生形态的 dECM 薄片。dECM 支架的宏观结构和微观形态受制于采集组织的结构,可能是片状或管状。目前扩大 dECM 支架应用的研究策略是探索水凝胶以及涂层和复合材料等组合装置。水凝胶提供了一种可注射的膨胀基质。然而,凝胶的制造需要酶解来溶解 ECM,这会使重要成分变性和失活,降低 dECM 的功能性生物活性。同样,dECM 涂层和复合材料可以改善机械性能或结构,但它们含有的替代材料会改变异物反应和组织重塑反应。需要一种方法来生产既能保持生物活性,又能调节几何形状,且不含会产生负面生物反应的添加材料的 dECM 支架。
电纺丝是一种可控制宏观和微观结构的制造平台,可按比例制造出具有临床相关尺寸的网格。例如,电纺丝材料可以制造出复杂的宏观结构,如瓣膜、移植物、敷料和包裹物。此外,还可控制纤维的微观结构,以改变各向异性、孔隙大小和表面纹理。例如,纤维可以排列以支持骨骼肌等各向异性组织的再生,也可以随机定向以支持脂肪组织等各向同性组织的再生。电纺丝网相互连接的多孔性和高表面积也为细胞的相互作用和渗透提供了一个可调的平台。尽管电纺丝有望制造出具有高生物活性保持力和多功能结构的 dECM 支架,但在电纺丝过程中使用聚合物添加剂来促进 dECM 纤维的形成仍然很常见。传统的电纺丝需要聚合物链的流动性,以便沿静电场排列,并需要链的缠结来承受静电力。聚合物添加剂可提高链的缠结性; 然而,添加剂会对支架的生物反应产生负面影响。其他增强可纺性的方法是利用酶消化法将 ECM 分解成单个链,这可能会因变性而降低生物活性。与消化和溶解 dECM 的传统纺丝溶液不同,我们最近的工作展示了一种使用脱细胞骨骼肌的新型悬浮电纺丝方法。从细胞附着、增殖和分化的角度来看,由此产生的支架保留了成肌生物活性。对 ECM 悬浮液进行电纺丝而不完全消化,有可能保持更高阶的蛋白质结构,从而使 ECM 支架具有更高的生物活性保持率和更慢的吸收率。控制和延长 ECM 支架的再吸收可以避免使用化学交联剂,因为化学交联剂会影响重塑并诱发慢性异物反应。然而,dECM 悬浮液的电纺丝技术刚刚起步,因此获得可纺丝悬浮液的关键流变学参数尚未阐明。要将电纺丝 dECM 支架的应用扩展到广泛的组织工程应用领域,需要对悬浮液的特性及其形成纤维的能力进行严格的评估。
本研究确定了促进电纺丝或灌输 “可纺性 ”所需的 dECM 悬浮液的关键特性。我们对各种 dECM 悬浮液进行了严格的流变学评估,这些悬浮液的均质化水平、浓度和磨碎颗粒大小各不相同,而 dECM 则来自 SIS。通过电纺不同成分的 ECM(由不同的脱细胞技术或组织来源制备),展示了 dECM 悬浮液电纺方法的多功能性。然后通过细胞增殖、巨噬细胞极化和血管生成评估生物活性的保留水平。对电纺丝 dECM 所涉及的关键参数进行评估,旨在为研究小组提供一个易于使用的工具箱,以创建具有高生物活性保留的专用 dECM 支架,用于多种组织再生应用。
二、摘要
脱细胞细胞外基质(dECM)作为组织工程支架具有强大的再生潜力;然而,目前临床上对脱细胞细胞外基质支架的选择仅限于将其原生形态冷冻干燥成薄片。电纺丝是一种多功能支架制造技术,可控制宏观和微观结构。对 dECM 进行电纺丝仍然具有挑战性,因此研究人员要么将其与合成材料混合,要么使用酶解法完全溶解 dECM。这两种方法都降低了 dECM 与生俱来的生物活性,限制了其再生潜力。在此,我们开发了一种新的悬浮电纺丝方法来制造纯净的 dECM 纤维网,并保留其固有的生物活性。通过对悬浮液参数的系统研究,我们确定了灌输 “可纺性 ”所需的关键流变特性,包括均质化、浓度和颗粒大小。均质化增强了颗粒之间的相互作用,从而赋予其必要的弹性行为,使其能够承受静电拉伸而不断裂。观察到浓度和粘度之间存在直接关联,从而改变了纤维形态;而颗粒大小对悬浮液特性和纤维形态的影响微乎其微。通过使用三种常见的脱细胞技术(Abraham、Badylak、Luo)和组织来源(肠粘膜下层、心脏、皮肤)对 dECM 进行电纺丝,证明了这种新方法的多功能性。电纺后的生物活性保留。
三、 结论
在本研究中,我们对支持电纺丝过程中纤维形成所需的 dECM 悬浮液特性进行了严格评估。均质化被用作增加颗粒相互作用和 dECM 悬浮液弹性行为的一种机制。损耗模量和存储模量曲线的交叉应变振幅超过 100%,被确定为可纺 dECM 悬浮液的功能性流变预测指标。纤维形态对悬浮液浓度的敏感性与电纺丝过程中聚合物溶液浓度的变化趋势相似。有趣的是,当悬浮颗粒分解成一致的状态时,纤维形态和纺丝相对独立于干燥颗粒的大小。通过利用三种不同的脱细胞和制备技术以及三种不同成分的 dECM 组织源,展示了这种 dECM 悬浮电纺丝方法的多功能性,这表明它有可能利用迄今为止只能制成粉末的组织源制造 ECM 支架,并模拟目标器官系统的原生 ECM 成分。这些组显示出类似的可纺性流变预测指标,即交叉应变振幅超过 100%。这些研究说明了 dECM 制备过程中每个步骤对纤维收集的影响,因此可以根据特定的组织来源和应用随时调整方案。我们开发这种新型悬浮电纺丝方法的主要目的是提高加工后网状物的生物活性保持率,这是目前使用合成聚合物混合物或酶消化的 dECM 纺丝方法的主要局限。研究表明,这些电纺 SIS 网在细胞增殖、血管生成和免疫调节方面的再生能力与脱细胞 SIS 片对照组相似。总之,这项研究阐明了指导 dECM 悬浮电纺丝的关键参数,为研究人员提供了一个框架,以利用这种新方法制造出保留其原生再生能力的 dECM 支架。
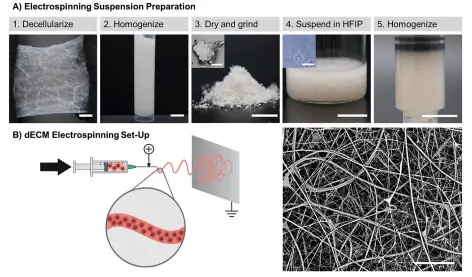
图1.dECM 电纺丝方法示意图。A) dECM 电纺丝悬浮液的制备分为五个步骤,包括脱细胞、均质化、研磨、在 HFIP 中悬浮和第二轮均质。步骤 1-5 的宏观图像;比例尺 = 1 厘米。步骤 3 中干燥 SIS 颗粒的嵌入式 SEM 图像;比例尺 = 300 μm。步骤 4 中悬浮 SIS 颗粒的内嵌明视野图像;刻度线 = 60 微米。B) 通过在流动的悬浮液和收集器之间施加电场,对 dECM 悬浮液进行电纺丝。图形由 BioRender 绘制。电纺 dECM 纤维的 SEM 图像;比例尺 = 30 μm。

图2.SIS 浓度对悬浮液流变特性和纤维收集的影响。A) 纤维形态的扫描电镜图像。比例尺 = 20 μm。

联系客服二维码

纳米纤维及其应用