联系我们
- 电话/微信:18520902353
- 客服QQ:3597831168
- 邮箱:info@wemaxnano.com
- 地址:广东省佛山市南海区狮山镇长兴西路12号建发风梅岭产业园9号楼
一、研究背景
近十年来,研究人员对骨组织工程的兴趣与日俱增,并广泛研究了制作骨诱导支架的不同方法。引导骨再生(GBR)是治疗严重骨缺损,尤其是颅骨缺损的常用技术。这些支架的基本原理之一是防止快速生长的软组织穿透密封的缺损区域,在其中起到机械屏障的作用。同时,这也确保了成骨细胞在受损区域增殖和分化的时间。传统的电纺丝是利用各种聚合物(天然或合成)制造 GBR 膜(GBRm)的一种简单技术。获得的膜具有柔韧性和生物可降解性,因此可以留在原位,无需二次手术取出。然而,由于这些膜缺乏骨诱导能力,而骨本身的再生能力不足,因此受伤后形成的新骨数量并不理想。因此,目前的研发计划主要集中在创造一种生物活性 GBRm,这种 GBRm 既能作为阻碍支架,又能提供生物活性成分,加速缺损部位的骨重组。
研究人员发明了一种使用纤维膜作为药物载体的独特方法。这种方法可将药物局部输送到目标部位,并显著改善膜下受保护空间中成骨细胞的功能。然而,通过电纺丝膜进行单次给药可能仍然不够。通常,在治疗的第一周,一些患者可能只需服用一次抗生素,而另一些患者则可能受益于成骨因子与细胞归巢因子的延迟和持续释放。为了解决这些局限性,随着纳米技术的发展,出现了双重给药系统。这些系统在同时递送两种药物方面表现出了卓越的能力。例如,Gentile 等人制作了负载纳米羟基磷灰石的电纺纳米纤维(NFs),然后使用逐层(LbL)方法对生物功能肽进行多层纳米封装,以模拟骨愈合的早期事件,包括血肿的形成和炎症细胞(中性粒细胞和巨噬细胞)的招募。他们还发现,在几天内,间充质干细胞(MSCs)开始迁移到骨折部位并分化。在另一项研究中,Wang 等人提出了一种核壳纳米纤维膜,它具有预防感染和促进骨生长的潜力。
考虑到骨组织再生过程,有两个基本步骤。首先是将成骨细胞祖细胞招募到损伤部位,其次是需要引起和改善成骨细胞的整体功能,以加速骨再生。在过去的几十年中,细胞归巢与成骨促进之间的联系引起了广泛关注。骨损伤后,最初的炎症反应包括中性粒细胞渗入受损区域,通过促炎和趋化信号招募第二波炎症细胞(如单核细胞、巨噬细胞和淋巴细胞等)。这些炎症细胞随后分泌的细胞因子和趋化因子会触发间充质干细胞(MSCs)和造骨细胞从各自的局部龛位向损伤部位迁移和募集。Liu等人研究了辛伐他汀(SIM)和基质细胞衍生因子1a对促进骨组织再生的不同影响。然而,在他们的研究中,对药物的输送方式缺乏深入了解,而且药物释放不受控制和/或无序。因此,潜在的研究空白可能是开发一种具有双重给药系统的分层纳米纤维膜,它能以可控和定制的方式释放细胞归巢因子和成骨因子。这种膜有可能优化早期细胞募集和骨形成之间的平衡。
在之前的研究中,我们通过共轭静电纺丝机成功制备了一种分层聚己内酯/明胶(PCL/GEL)静电纺丝膜,该膜能够以可调节的方式释放两种不同的药物。膜中的 PCL 可间接调节 GEL 的降解,从而使药物从亲水性 GEL 纤维中的初始释放和随后从疏水性 PCL 纤维中的连续释放变得可调,从而形成一种基于共聚物的复杂多功能给药系统。在此基础上,我们计划在本研究中设计一种由负载物质P(SP)的GEL纤维和负载SIM的PCL纤维组成的共轭静电纺丝膜,采用细胞归巢法加强细胞招募,促进成骨祖细胞分化。SP 是一种神经肽,最初由外周感觉神经纤维分泌,属于速激肽神经肽家族。它与受体 1 型神经激肽(NK-1R)结合,这种受体存在于人体内的多种细胞类型中,包括淋巴管、成纤维细胞、血管内皮细胞、白细胞和神经元。之前的一项研究显示,损伤可激活 SP,使其成为一种信使,促使人体自然修复机制,进而招募间充质干细胞(MSCs)并将其迁移到受损部位。
SIM 是一种用于降低胆固醇和减少心血管疾病风险的药物。最近的研究还表明,SIM 除了具有降低胆固醇的作用外,还具有其他治疗功效。具体而言,研究发现 SIM 能促进血管生成,而血管生成对骨再生和组织修复非常重要。例如,Bitto 等人称 SIM 能增加血管内皮生长因子(VEGF)的表达,促进内皮细胞迁移和管形成,从而增强血管生成。Pullisaar等人证实,与不含SIM的人脂肪组织间充质干细胞(hAD-MSCs)相比,SIM能增强在含SIM的支架上培养的人脂肪组织间充质干细胞中成骨细胞相关基因的表达和几种成骨标志物的分泌,包括骨蛋白激酶(OPG)、血管内皮生长因子A(VEGFA)、骨生成素(OPN)和骨钙素(OC)。这些结果表明,SIM 对血管生成和成骨具有积极作用,可能具有作为组织再生治疗剂的潜力。
因此,受细胞外基质(ECM)结构和自然骨愈合过程的启发,我们以负载 SP 的 GEL 作为纳米纤维(易降解),以负载 SIM 的 PCL 作为微纤维(相对较难降解),旨在制造一种分层 PCL/GEL 膜。共纺膜的设计目的是在两周内持续释放 SP。同时,PCL 的缓慢降解可使 SIM 的持续释放时间超过一个月,从而确保在新骨形成之前持续诱导成骨。如方案 1 所示,当前工作的目的如下: 1)开发一种负载 SIM 和 SP 的生物活性膜;2)评估其对早期细胞招募的生物效应,并研究其对体外和体内血管生成和成骨的影响。
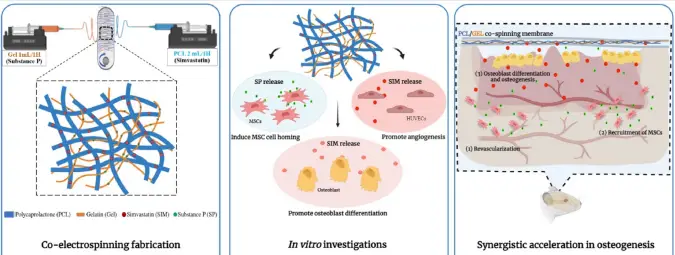
图1.共轭静电纺丝膜的组成及其对体外和体内早期细胞募集、血管生成和骨生成的生物效应示意图。
二、摘要
骨再生是一个复杂的过程,需要协调各种生物事件。开发一种能调节这一系列事件的组织再生膜具有挑战性。在这项研究中,我们的目标是制造一种膜,它能用间充质干细胞丰富受损区域,改善血管生成,并持续诱导骨生成。我们的方法是通过共轭静电纺丝机制造一种分层的聚己内酯/明胶(PCL/GEL)共轭静电纺丝膜,其中包含负载物质P(SP)的明胶纤维和负载辛伐他汀(SIM)的PCL纤维。该膜可启动 SP 的猝发释放和 SIM 的缓慢/持续释放,持续时间超过一个月。体外实验,包括与血管生成和成骨相关的实验(如迁移、内皮网络形成、碱性磷酸酶活性、矿化和基因表达),清楚地证明了该膜在改善细胞归巢、血管再形成和成骨分化方面的卓越能力。此外,一系列体内研究,包括 CD29+/CD90+ 双阳性细胞的免疫荧光以及 CD34 和 vWF 的免疫组化染色,都证实了共轭静电纺丝膜在植入五天后增强间充质干细胞迁移和血管再形成反应的能力。一个月后,Micro-CT 和组织学(Masson 和 H&E)结果显示骨再生加速。我们的研究结果表明,具有时间可调药物递送功能的共轭静电纺丝膜能在短时间内提高间充质干细胞的迁移和血管再形成反应。
三、结论
综上所述,静电纺丝技术成功制备了一种具有可调药物释放功能的分层双重给药系统(PCL-sim/GEL-sp)。一系列体外细胞实验表明,PCL-sim/GEL-sp膜能有效促进HUVECs的迁移/血管生成和间充质干细胞的募集/骨细胞分化。此外,包括免疫组化染色、显微 CT 扫描观察和 H&E/Masson's trichrome 染色在内的体内结果进一步表明,PCL-sim/GEL-sp 膜能显著刺激细胞募集、血管再形成和骨生成,从而加速骨再生过程。总之,我们的研究结果增进了我们对共轭静电纺丝膜的了解,并为潜在的临床应用奠定了基础。
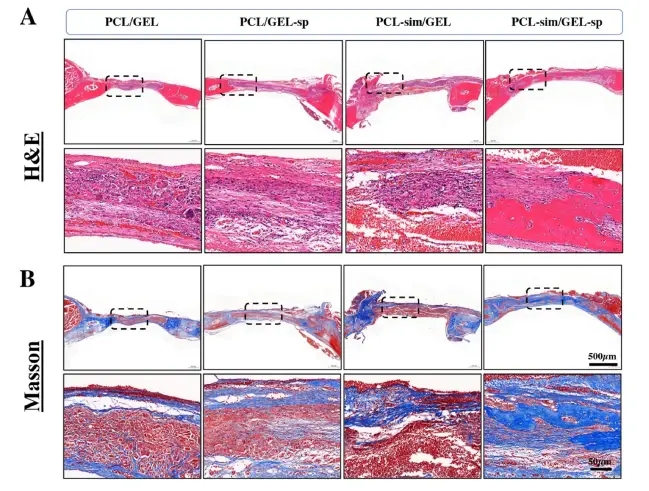
图2.植入一个月后骨缺损区域的组织学分析。(A) 小腿骨缺损的 H&E 和 (B) Masson 三色染色图。

联系客服二维码

纳米纤维及其应用