联系我们
- 电话/微信:18520902353
- 客服QQ:3597831168
- 邮箱:info@wemaxnano.com
- 地址:广东省佛山市南海区狮山镇长兴西路12号建发风梅岭产业园9号楼
一、引言
二、核心内容
1、水凝胶纤维制造的常用材料
2、水凝胶纤维的结构设计
3、水凝胶纤维的制造技术
4、水凝胶纤维的应用场景与性能考量
5、水凝胶纤维的功能与应用
三、图文解析
四、总结与展望
水凝胶纤维(Hydrogel Fibers, HFs)是近年来受到广泛关注的一类先进材料,它们在生物体中广泛存在,如肌肉、神经和结缔组织,能够传输物质和能量,通过协作的自下而上构建实现重要的生命功能。正是基于其在生命体中的丰富存在和重要功能,开发能够紧密模仿生物功能的HFs显得尤为重要。HFs以其高含水量和纤维状形态为特征,内部具有交联网络,兼具水凝胶材料的柔软、湿润、环境响应和生物相容性等功能特性,以及纤维材料的高长径比、各向异性、柔韧性等结构优势。这种独特的组合使得HFs在生物医学、能源和环境科学等领域具有巨大的应用潜力。
水凝胶材料的历史可以追溯到19世纪末20世纪初,最初用于描述无机盐胶体。随着领域发展,“水凝胶”一词现在主要指能在水或生物液体中溶胀的物理或化学交联聚合物。从20世纪50年代到90年代,水凝胶的研究主要集中在拓展原材料、控制网络结构和分析基本性质(如溶胀和力学性质)。进入90年代和21世纪初,湿法纺丝技术促进了HFs的发展,并广泛应用于环境响应和驱动领域。随后,HFs进入了快速发展时期,结构从单一发展到多重,包括长丝、纳米纤维膜以及其他多重结构。同时,HFs的功能也日益多样化,包括材料运输、导电性和光学性能等。这些进步极大地拓展了HFs的应用领域,使其可用于信号传感、组织修复、仿生过程等。这篇综述旨在提供构建功能性或仿生HFs及其实际应用的指导。
东华大学朱美芳院士、侯凯教授团队在《Chemical Reviews》上发表题为“A Review of Hydrogel Fiber: Design, Synthesis, Applications, and Futures”的综述论文,系统梳理了水凝胶纤维领域的最新研究进展。文章全面总结了材料选择、结构设计、制备方法及应用拓展等关键内容,为该领域未来的基础研究与应用开发提供了重要的理论指导和技术参考,推动水凝胶纤维在生物医学、柔性电子、能源存储、环境治理等多个方向的深入应用与发展。
1、水凝胶纤维制造的常用材料
HFs的原材料根据来源和特性可分为天然聚合物、合成聚合物、单体/低聚物和纳米粒子。这些原材料对HFs的加工和性能控制至关重要,不同的原材料表现出不同的特性(如分子量、亲水性、结构可设计性)、功能(包括环境响应和传输性能)和交联机制(如离子键、氢键、范德华力)。
1.1天然聚合物
例如海藻酸钠(NaAlg)、壳聚糖、纤维素、明胶、琼脂糖、角叉菜胶、透明质酸(HA)和蛋白质(如蜘蛛丝、桑蚕丝)、脱氧核糖核酸(DNA)等。
(1)优点:亲水性、生物相容性、生物可降解性和高分子量。
(2)亲水性:富含亲水性官能团(如羟基、羧基、氨基),可形成强相互作用(离子键、氢键、范德华力等)构建3D网络,并提供丰富的反应位点进行分子修饰,从而实现可控交联。
(3)生物相容性:提取自天然来源,如植物和动物,具有固有的生物相容性,常用于生物材料制造,如丝素蛋白(SF)用于可植入HFs,琼脂糖用于软骨修复和神经再生。
(4)生物可降解性:主链通常由酯、醚、酸酐、酰胺等易生物降解键连接,降解机制主要为水解和酶降解。降解速率可通过调节天然聚合物含量、交联度和分子量来控制。
(5)高分子量:大多数天然聚合物具有高分子量,有利于在溶液加工过程中形成牢固的分子链缠结,适用于HFs的连续纺丝。
1.2 合成聚合物
通过人工聚合单体合成,易于获得,通常表现出高稳定性和优异的机械性能。
(1)优点:链柔韧性、高线性和亲水性。
(2)链柔韧性与高线性:主链主要由单键组成,立体阻碍小,有利于分子链在水凝胶网络中的运动和结晶形成,尤其适用于短时间纤维成型过程中的连续纺丝。
(3)亲水性:富含亲水性基团,促进分子间或分子内氢键形成,常用于构建多重交联网络以增强水凝胶强度。也可赋予环境响应性,如NIPAM用于制备温敏HFs,PAA用于pH响应HFs。
(4)功能可设计性:在合成过程中通过精确控制参数(如进料比、反应时间)来调节功能特性,如温度响应点和分子量。可引入大环化合物(如葫芦脲、环糊精)形成动态交联结构,赋予自修复性能和特定功能(如pH响应性、温敏性、载药能力)。
1.3 单体/低聚物
通常不涉及凝胶化过程中的聚合,交联通常不基于共价键,对网络强度和可设计性有一定限制。高性能HFs可通过丙烯酸(AA)、丙烯酰胺(AAm)、二甲基丙烯酰胺(DMAAm)、聚乙二醇二丙烯酸酯(PEGDA)等单体或低聚物制备。这些材料主要通过自由基聚合形成水凝胶网络。
(1)优点:结构可设计性和功能性质的精确控制。通过调节交联剂用量可精确控制交联度,影响溶胀稳定性和机械性能。通过调节组分可精确控制环境响应功能,如调节NIPAM与AAm的浓度比来调节温敏HFs的LCST。
(2)可控生物可降解性:水凝胶网络可设计性强,通过在分子骨架中引入易降解键或共聚促进降解的官能团,可精确控制降解速率。
(3)局限性:由于小分子在凝固浴中扩散,以及聚合反应的耗时性与快速纤维成型要求的矛盾,不适用于常规的连续纺丝。需要多场协同纺丝方法(如UV光和热环境)。
1.4、纳米粒子
用于增强网络和功能多样性,灵感来源于生物体中骨骼的复合结构。
(1)亲水性纳米粒子:如粘土、纤维素纳米晶体(CNC),表面富含亲水性基团,可与水凝胶网络形成强相互作用并作为交联剂,增强机械强度和溶胀性能。
(2)导电纳米粒子:如氧化石墨烯(GO)、碳纳米管(CNT)、聚苯胺(PANI)、聚(3,4-乙烯二氧噻吩):聚(苯乙烯磺酸盐)(PEDOT:PSS)、银纳米线(AgNWs)、液态金属。常用于构建导电HFs,但分散性是关键挑战。
(3)磁响应纳米粒子:如氧化铁纳米粒子(Fe3O4),可赋予HFs磁响应性,用于靶向药物递送、软机器人和医学诊断。
(4)分子敏感纳米粒子:响应金属离子(Fe3+、Pb2+)和功能分子(葡萄糖),适用于环境监测和传感。
(5)抗菌纳米粒子:非金属(碳基)和金属基(Ag、Au、CuO、ZnO)纳米粒子,用于制备抗菌HFs,但需考虑细胞毒性。
(6)加工性增强:亲水性纳米粒子可显著增强预凝胶溶液的粘弹性,确保纤维成型。
综上所述,原材料的选择(如溶解度、凝胶机制、多网络构建和纳米填料的分散性)对HFs的制备过程、纤维成型和水凝胶网络交联至关重要。对于连续大规模生产,天然聚合物因其快速凝胶化和长链结构而常被选作主要原材料或纺丝助剂。
2、水凝胶纤维的结构设计
HFs的结构和功能是决定其应用场景的关键因素。仿生设计是HFs发展的重要方向,例如肌肉的层次结构启示了HFs的多尺度结构设计。通过自下而上的组装和结构设计方法,有望制备出具有所需性能的HFs。
2.1精确的微观结构设计
(1)交联结构的选择:
▪共价键:永久性(不可逆,键能高)和动态共价键(可逆,自修复)。可调节交联点间距来控制HFs的模量、弹性和含水量。
▪配位键:电子供体(有机配体)与受体(金属离子如Zn2+、Fe3+、Ca2+、Co2+)之间的相互作用。可与弱相互作用结合增强韧性。
▪静电相互作用:正负电荷基团之间的弱相互作用。适用于快速凝胶化的连续纺丝过程。
▪氢键:较弱的物理相互作用,可逆,赋予HFs自修复和高机械性能。
▪疏水缔合:疏水力形成,具有一定动态可逆性,作为物理交联点,赋予HFs更强的断裂强度、更大伸长率和更低的溶胀率。
▪主客体相互作用:基于空腔主体分子和大小合适的客体分子之间的瞬态结合,具有动态结构,赋予HFs自修复能力并增强机械强度。
(2)溶剂相的调控:HFs中溶剂含量可达90%,其状态和性质直接影响HFs的理化特性。
▪溶剂分子-聚合物链相互作用:添加富含亲水或极性基团的有机小分子溶剂(如甘油、三甘醇)可增强交联网络内的分子间作用力。
▪溶剂分子间相互作用:通过添加有机溶剂(如乙二醇、甘油)或无机盐离子/离子液体,可降低水的冰点、抑制水蒸发和结晶,从而构建抗冻和抗挥发HFs。
(3)功能相的构建:
▪导电性:离子导电:通过引入盐离子(如Li+、Na+、Ag+、Ca2+)或离子液体,或选择带电聚合物作原材料5354。导电性能相对有限。电子导电:通过掺入导电纳米粒子(如CNTs、rGO、PEDOT:PSS、AgNWs),形成导电通路,可均匀分散纳米粒子或工程化连续相结构(如表面涂层、冷冻铸造)。后者的导电率可达1×10^4 S/m以上。
▪光学透明性:透明的水凝胶相是制备高导光性HFs的基础。采用纯相单体或聚合物制备,确保网络结构单相或缺陷少,避免结晶、纳米粒子和不均匀链聚集影响透光性。
▪物质储存:水凝胶多孔网络结构可用于药物递送、吸附污染物和细胞封装。药物释放可通过网络密度、特定相互作用或外部刺激进行控制。
▪热响应性:基于温度高于LCST时分子链中疏水链段聚集引起的相分离现象,导致HFs物理性质(体积、透光率)变化,用于温度传感和驱动。
▪分子响应性:通过官能团或功能单元的接枝、共聚或杂化,使HFs对葡萄糖、碘离子、酸碱离子、金属离子等分子敏感,用于医学诊断和环境监测。
▪湿度响应性:HFs吸湿脱湿过程导致内部交联密度变化,从而改变物理性质。通过构建高亲水性和吸湿性网络,结合导电或光导性实现湿度监测。
▪磁响应性:掺入磁响应纳米粒子(如Fe3O4)赋予磁响应性,实现非接触远程驱动、磁热转换或感应耦合磁性,应用于靶向药物递送、软机器人和医学诊断。纳米粒子的分散和定向排列是挑战。
▪抗菌性能:通过选择具有抗菌性能的原材料(如壳聚糖)、抗菌纳米粒子或溶剂(如甘油)来实现。
2.2介观结构组装
(1)多重交联网络:单网络HFs机械性能较差。通过构建双网络或更高阶多网络(如脆性与韧性网络、共价与静电网络),显著提高断裂能、强度和韧性。可结合导电相作为第三网络,同时增强导电性和机械性能。
(2)均匀网络:对于纯聚合物网络,均匀网络对提高透光率、温敏响应和机械性能至关重要。可选用亲水性单体、星形聚合物或具有移动交联点的聚合物。对于聚合物与纳米粒子复合的HFs,纳米粒子的均匀分散是关键。可通过表面功能化(如修饰亲水基团)或使用表面活性剂(如两亲性分散剂)来改善分散性。
(3)聚集结构:包括结晶结构和无定形区,影响HFs的宏观性能。如PVA基HFs通过冷冻-解冻循环或盐溶液浸泡可提高结晶度,显著增强机械强度和抗疲劳性。退火处理也可增加结晶度,改善抗疲劳性和光学性能。
(4)取向结构:受生物组织中纤维排列启发,通过引入外场(如拉伸力场、流体力场、速度场、磁场)实现HFs内部聚合物链、晶区、纳米粒子、多孔结构和微纤维的取向。
▪拉伸力场:在纺丝或成型后施加,使分子链取向排列,提高机械性能。
▪流体力场:溶液通过纺丝通道时,层流现象使纳米粒子和多孔结构取向,对聚合物分子链取向影响有限。
▪速度场:静电纺丝中,通过收集装置的转速差诱导微纤维取向,适用于促进细胞定向生长。
▪磁场:主要用于磁响应纳米粒子的取向,可与挤出成型结合或在聚合前对预凝胶溶液进行取向。
2.3 多重宏观结构构建
(1)中空结构HFs:具有管状腔体,用于定向物质传输(药物、溶液)、细胞定向生长等。可通过共轴流体通道挤出成型(湿法纺丝、微流控纺丝、3D打印)实现。
(2)核壳结构HFs:两种不同组分呈核壳构型,可集成不同材料的优势,如利用折射率差异实现优异导光性。核壳层可独立功能化,实现多结构多功能。可通过共轴湿法纺丝、微流控纺丝或涂层技术制备。
(3)多核壳结构HFs:具有多个核层,可用于多种药物协同释放、光电集成探针等。通过增加核心通道数量或组装多种功能纤维材料实现。
(4)并排结构HFs:两根或多根HFs平行排列形成纤维束或膜,保持纤维各向异性并赋予特殊功能(如组织再生、多药物释放、驱动响应)。可通过并排挤出装置或纤维成型后平行排列实现。
(5)Junas结构HFs:并排结构HFs的特殊形式,由两种或多种不同结构或功能的HFs构成,沿纤维轴向呈不对称结构或功能。可实现环境敏感响应,用于驱动器构建。
(6)螺旋结构HFs:模仿植物藤蔓,赋予HFs高机械性能和驱动能力。可通过扭曲多股HFs、设计专用喷嘴或将HFs缠绕在圆柱体上固化实现。
2.4 界面相互作用策略
稳健的界面结合对于多重结构HFs的长期性能至关重要。
(1)纳米粒子/聚合物界面:亲水性纳米粒子(如纳米粘土、CNC、GO)可与亲水性聚合物网络形成良好界面。对于缺乏亲水基团的功能性纳米粒子(如导电、抗菌纳米粒子),可通过表面功能化(修饰双键或亲水基团)或使用两亲性分散剂来增强界面结合。
(2)不同HFs间的聚合物/聚合物界面:在构建并排或螺旋结构时,可引入可形成动态交联的原材料(如氢键、主客体相互作用),或采用同步交联方法实现不同HFs间聚合物网络的整体成型。
(3)单个HFs内部的聚合物/聚合物界面:在核鞘或多核鞘结构中,通过共聚、接枝或混合,在不同层间形成氢键、共价键和缠结等桥接作用力,确保界面粘附性。
3、水凝胶纤维的制造技术
HFs的制造主要包括纤维成型和凝胶化两个关键过程。
3.1 凝胶化机制
(1)溶剂挥发诱导分子间相互作用:水分子蒸发促进分子链间相互作用(静电、氢键、疏水缔合)形成交联网络。适用于干法工艺,要求预凝胶溶液粘度高以维持纤维形状。
(2)溶剂状态诱导分子聚集:将预凝胶溶液注入凝固浴进行溶剂萃取或低温处理进行溶剂冷冻,导致分子聚集并形成HFs。适用于湿法纺丝和微流控纺丝,要求聚合物具有高分子量以形成有效缠结。
(3)扩散驱动的物理/化学交联:金属离子、酸/碱离子扩散到新生HFs中诱导凝胶化,形成物理(静电、氢键)或化学(可逆共价键、配位键)交联结构。适用于湿法纺丝、微流控纺丝和动态交联法。
(4)聚合主导的HFs成型过程:单体/低聚物通过聚合反应在限定空间(纤维状空间)内构建交联网络。光聚合因其聚合速率可控、条件简单易操作、反应效率高而被认为是一种有潜力的连续制备HFs的方法。
3.2 HFs成型方法
(1)凝胶化前成型:从已形成的水凝胶材料中制备HFs,通过破坏网络结构或扭曲方法(如挤出法、切割法、膜扭曲法)降低尺寸。这些方法通常是非连续的,生产受限。
▪挤出法:将预交联的水凝胶通过孔结构挤出,破坏3D网络,获得1D纤维。
▪切割法:将水凝胶膜切割成长条,然后扭曲或拉伸获得HFs。
▪膜扭曲法:直接将水凝胶膜通过机械或手动扭曲成纤维状。
(2)纤维成型后凝胶化:交联网络在纤维成型后构建,交联过程必须在限定空间内进行。
▪模板法:将预凝胶溶液置于纤维状模具中(如毛细管),原位聚合形成交联网络,脱模后获得HFs。
▪涂层法:利用已制备的纤维作为空间模板,将预凝胶溶液涂覆在纤维表面形成薄层,凝胶化后获得多重结构HFs(通常为核鞘结构)。该方法可赋予HFs多种功能,但需注意界面结合性能。
▪静电纺丝:通过高压电场将纺丝溶液连续拉伸,在接收器上形成2D纳米纤维膜,之后构建交联结构。可制备无序或有序的微/纳米尺寸纤维集合体。对纺丝溶液粘弹性要求高,不适用于低粘度单体/低聚物作原材料。对静电纺丝行业而言,这是制造具有分层取向结构和优异生物相容性HFs的关键技术,尤其适用于神经修复等领域,因为快速缠绕收集装置能获得取向纳米纤维,对驱动器器件构建具有重要作用。
▪浓缩溶液拉伸法:直接从聚合物浓缩溶液中拉伸,通过溶剂挥发诱导相分离形成HFs。适用于高分子量聚合物,在构建取向结构和增强机械强度方面具有优势。
▪动态聚合辅助拉伸纺丝技术:近年发展起来的技术,在预凝胶溶液中引入纳米粘土调节粘度,并在系统自由基聚合过程中施加拉伸力,形成高度交联网络和高度取向的HFs。该方法有望实现HFs的连续生产。
(3)纤维成型同时凝胶化:旨在解决网络构建和纤维成型在时间和空间上的矛盾,实现HFs的连续制备。
▪3D打印:挤出打印通过挤出预凝胶溶液并自组装或后交联形成HFs,要求精确控制预凝胶溶液的粘弹性。溶液书写(数字光处理DLP)则利用UV光斑诱导单体聚合,实现HFs的连续添加固化。
▪微流控纺丝:利用微流控芯片控制微尺度流体,在双层或多层通道结构中,核心层预凝胶溶液与鞘层惰性液体同时挤出,通过化学或物理相互作用同步凝胶化和成型。该技术可控制流体参数,实现螺旋结构HFs和取向结构HFs的制备。虽然微流控纺丝可以连续构建HFs且尺寸均匀、可控,但其微通道的复杂性和制备工艺限制了工业化应用,实验要求高且成本昂贵。
▪湿法纺丝:工业化生产纤维材料的常用方法,通过纺丝喷嘴将聚合物纺丝液挤入凝固浴,利用扩散驱动的交联作用使纤维丝固化成型,并伴随拉伸。不适用于单体/低聚物,主要原材料为高分子量成纤聚合物。可通过控制拉伸挤出速度比实现微观结构(如分子链、纳米粒子)的取向。
▪动态聚合纺丝:近年新出现的方法,将UV光源设备安装在纺丝喷嘴或附近,使预凝胶溶液在纤维成型和凝胶化同步进行。可实现单体/低聚物直接纺丝制备HFs,具有连续大规模生产和快速纤维生产的优点。适用于快速聚合体系。
3.3 已制备HFs的后处理
(1)再交联:针对连续制备过程中单体/低聚物聚合不完全的问题,通过后续再交联处理(如浸入引发剂溶液并加热)完善凝胶网络完整性,增强HFs强度。
(2)后功能化:主要针对导电性,通过涂层技术在HFs表面构建功能层(如AgNWs涂层),或将功能单元引入凝胶纤维网络结构内部(如将ANI扩散到网络中原位聚合形成PANI)实现导电性能。
(3)纺织加工技术:HFs可通过扭曲、编织或非织造工艺加工成各种形式,以适应不同应用需求。
▪扭曲技术:将多股HFs扭曲成螺旋结构,增强纤维强度和驱动特性。
▪编织技术:通过交错或钩编纤维材料,形成结构化图案,可用于构建柔性电子设备或驱动器,实现二维或三维压力传感。对于静电纺丝领域,将微/纳米纤维膜通过后处理(如切割、扭曲)或直接纺织(如编织成布)是实现复杂功能(如定位检测、3D压力传感、生物传感器)的重要途径。
▪非织造加工:将HFs加工成短纤,再通过混合、热轧等工艺制成水凝胶非织造纤维,应用于敷料(如高吸水性、高透气性)。
4、应用场景的性能考量
HFs的性能决定了其应用,而性能又源于其结构。关键性能包括含水量、机械性能、生物相容性和可降解性。
4.1 含水量
HFs的决定性特征,影响性能和功能。高含水量通常意味着较低的机械强度。在高湿度或生理环境中,HFs的性能稳定性需考虑吸水引起的溶胀。在体内应用中,可设计不同含水量的HFs以匹配植入部位的机械模量。水分子易挥发导致长期使用稳定性差。可通过调节溶剂体系(添加离子液体、甘油、盐)或构建疏水表层防止水分蒸发。
4.2 机械性能
(1)提高断裂强度和弹性:通过调节化学组分(构建异质或多重交联网络、利用多臂交联点提高网络均匀性、利用纳米粒子或超分子滑环结构耗散能量)和物理结构(构建取向结构和结晶结构)实现。
(2)模量调节:HFs的模量与生物软组织(如大脑组织、肌肉、皮肤、软骨)相似。可设计特殊结构(如取向结构、纳米复合结构)以匹配不同组织模量,避免植入物与组织界面处的机械不匹配导致炎症和异物排斥。
4.3 生物相容性
HFs用于生物医学领域时(如生物传感器、药物递送、组织工程),生物相容性至关重要,包括低细胞毒性、低过敏性和长期稳定性。
(1)原材料选择:天然聚合物(如多糖基、蛋白基聚合物如壳聚糖、明胶)具有优异生物相容性和生物功能性。合成聚合物(如PVA)也具有良好生物相容性。部分合成聚合物本身缺乏生物相容性,但可通过修饰或复合加工改善。
(2)形态影响:取向结构HFs对细胞增殖、粘附和迁移有重要影响,可用于修复受损组织。网络孔径大小影响细胞渗透。
4.4 生物可降解性
(1)对于短期植入材料(如组织修复),生物可降解性至关重要,避免二次手术损伤,且降解产物无毒。天然聚合物或某些合成聚合物可作基质材料。
(2)可控降解:可通过在分子骨架中引入适当的降解位点或通过引入肽键实现酶降解来调节材料的降解周期。
(3)对于需要长期稳定植入的应用,则需选择非生物可降解材料(如碳-碳单键主链合成聚合物)。
5、水凝胶纤维的功能与应用
HFs结合了水凝胶的功能特性和纤维的结构优势,通过多重结构设计和功能构建,可开发出满足特定应用要求的功能集成HFs。
5.1 基于响应性的传感/驱动
(1)柔性应变传感:将外部应变转化为电信号或光信号的变化,用于实时监测生理健康指标(体动、心率、呼吸节律)。多重交联网络可改善循环恢复特性。HFs后处理和编织可实现高维应力传感。
(2)环境监测:
▪温度响应:利用温敏HFs的体积、透明度变化或导电/导光性质变化进行温度传感。
▪湿度响应:通过吸湿和脱湿引起内部交联密度变化,结合导电/光导性实现湿度监测。
(3)分子检测:利用HFs开放网络结构使分子进入网络并影响信号传输,实现对pH、血糖、重金属离子等分子的实时监测。
(4)HFs基驱动器:响应外部环境变化而改变形状,用于软机器人和仿生机器人。通常需要各向异性结构,通过混合磁性纳米粒子或构建偏心结构、并排结构、螺旋结构实现。
▪磁响应软机器人:HFs可作为磁响应软机器人的材料,用于复杂狭窄管道环境的探索或通过。
▪仿生机器人:利用HFs快速响应刺激的特性,结合响应功能和多级各向异性结构,模仿动物/纺织品的器官或组织功能,实现对温度、湿度、pH、光的变形响应。
5.2 基于孔隙率的能量/物质储存
(1)电能储存:HFs具有优异的柔韧性、可调孔隙率、导电性和离子传输能力,适用于制备柔性储能器件。可构建多层结构(阳极、电解质、阴极)用于纤维电池(超级电容器、锂电池、锌电池、铝电池)。HFs作为电极材料关注导电性和孔隙结构,作为电解质关注离子传输性能和提供机械支撑。
(2)药物释放:HFs比其他水凝胶材料具有更大的比表面积和内部孔隙率,适用于药物载入和释放。可实现单药物的持续释放,也可通过多层结构实现多药物的协同释放。
(3)水处理:HFs独特的3D多孔结构和高亲水性使其广泛应用于水处理。
▪吸附和催化降解:提供高活性位点,通过离子交换、配位或掺杂催化剂实现重金属离子、有机污染物的吸附和催化降解。
▪孔径控制:纳米纤维膜形式的HFs通过控制孔径物理截留病原体或污染物,实现高效过滤和油水分离。
5.3 基于电子/光学传输的医疗应用
(1)电生理检测与治疗:HFs优异的生物相容性使其可作为生理电极,用于收集生理电信号(脑电图、肌电图、心电图),诊断疾病。导电HFs具有高电导率和电荷存储容量,可实现神经信号的快速传输和有效记录。
(2)深层组织光医学:光导性HFs可将体外激光传输到深层组织进行光医学治疗(如光热癌症治疗),克服传统激光穿透深度限制。结合温敏性HFs可实现治疗过程的温度监控和智能关断。
(3)神经调控:通过光和电刺激目标神经元以调节神经细胞活动,结合生理信号记录提供反馈。HFs可作为电流和光信号的介质工具,实现高精度的神经调控,相比传统光纤和玻璃光纤具有更优异的生物相容性。可开发多功能HFs探针,同时进行神经活动记录和光遗传刺激。
5.4 基于生物相容性的组织工程
HFs的柔软性和含水性使其成为细胞生长和分化的理想细胞外基质材料。
(1)组织修复:通过植入敷料或组织工程支架,利用HFs的微纳米取向结构、机械性能调控或加载生长因子、干细胞等促进组织修复。
(2)体外组织重建:多重结构HFs可实现精确的组织重建,如血管、神经、肌肉组织的重建,模仿其固有的形态和功能。也可用于构建体外组织模型进行药物筛选。
(4)仿生组织:利用HFs的纤维状、机械性能和多重结构,仿生开发人造肌肉、韧带、肌腱、血管等替代功能缺陷组织。通过结构调控(取向、结晶、宏观螺旋结构)实现高强度、韧性、弹性和抗疲劳性。
图文解析
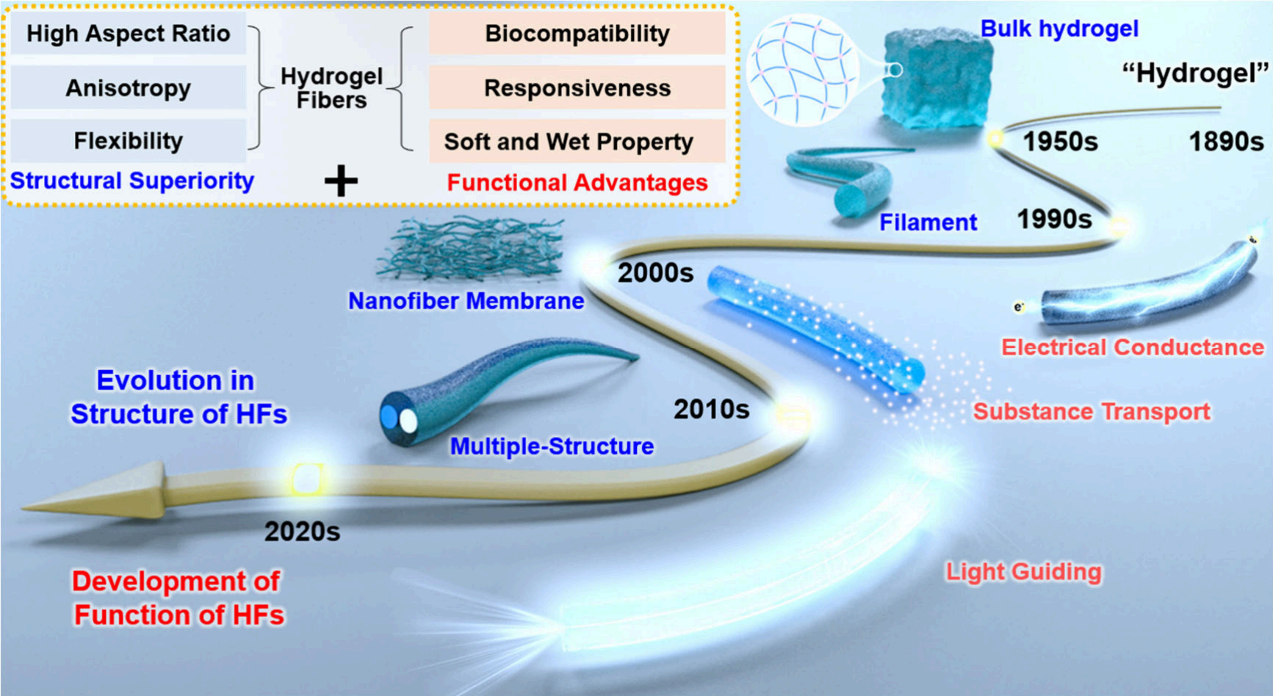
图1:展示了水凝胶纤维(HFs)从单一结构向多样化、多功能化演变的发展历程,包括纳米纤维膜、多核-鞘结构等,并指出其应用从最初的传感器扩展至生物医用领域
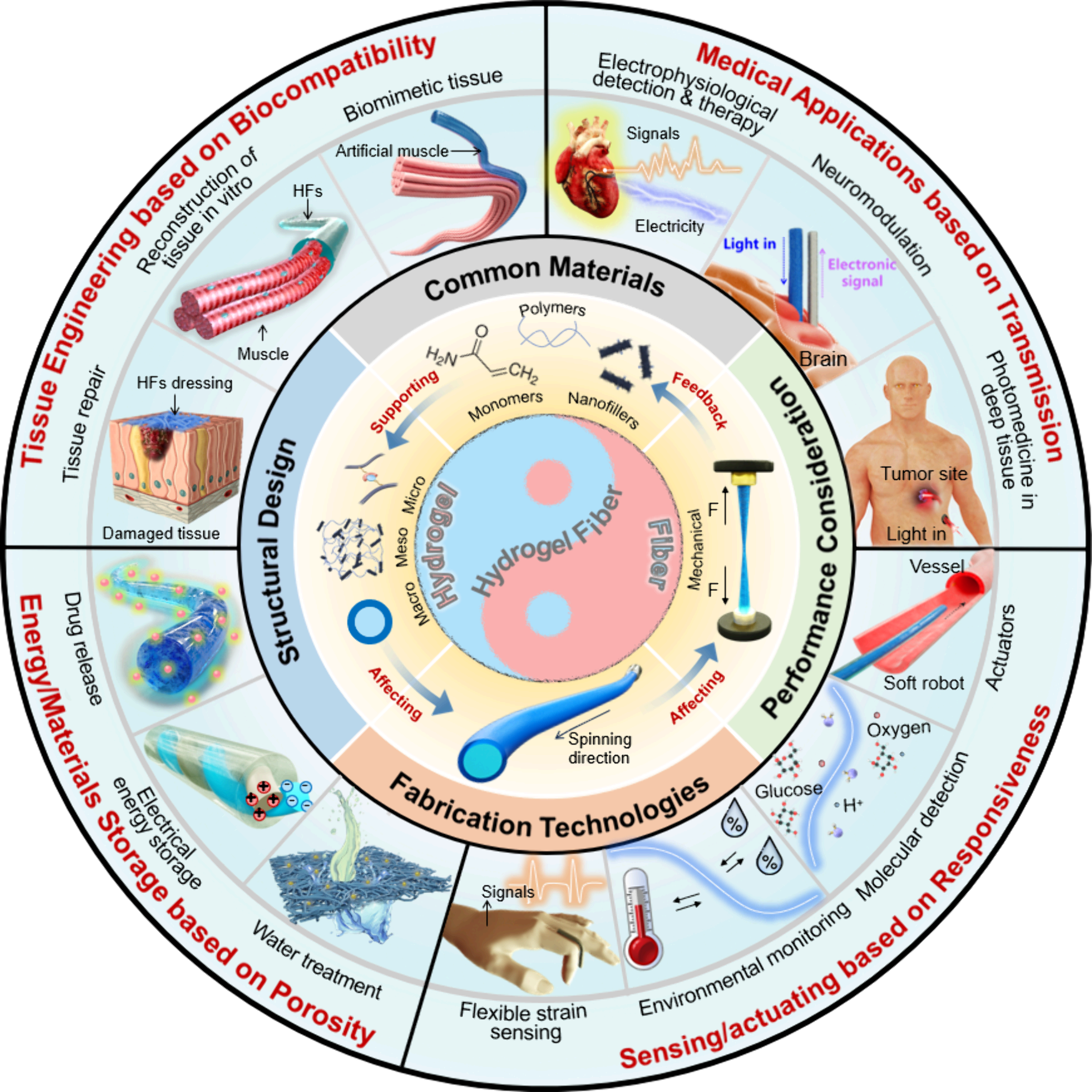
图2:概括了HFs从原材料选择、结构设计、功能构建到应用场景的全过程,强调了材料、制备技术与应用性能之间的内在联系
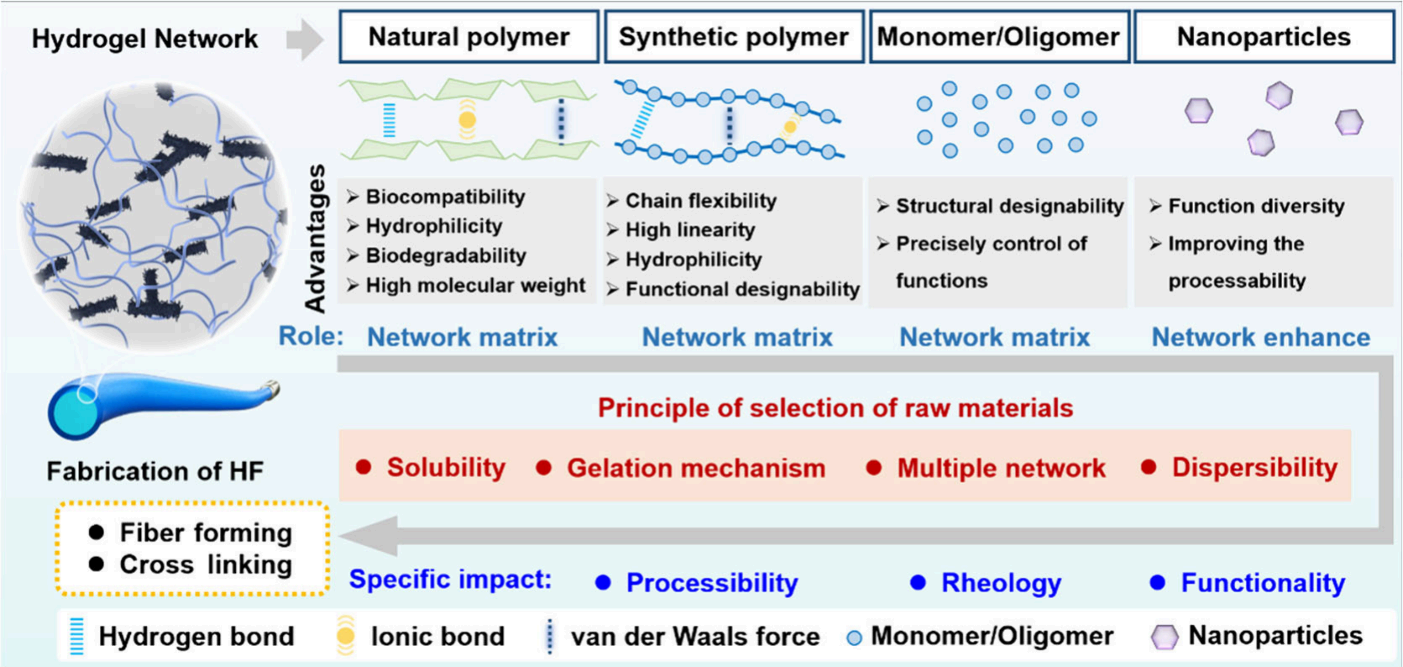
图3:总结了HFs常用的原材料分类,包括天然聚合物、合成聚合物、单体/低聚物以及纳米颗粒,并分析了它们对HFs结构与功能性能的影响
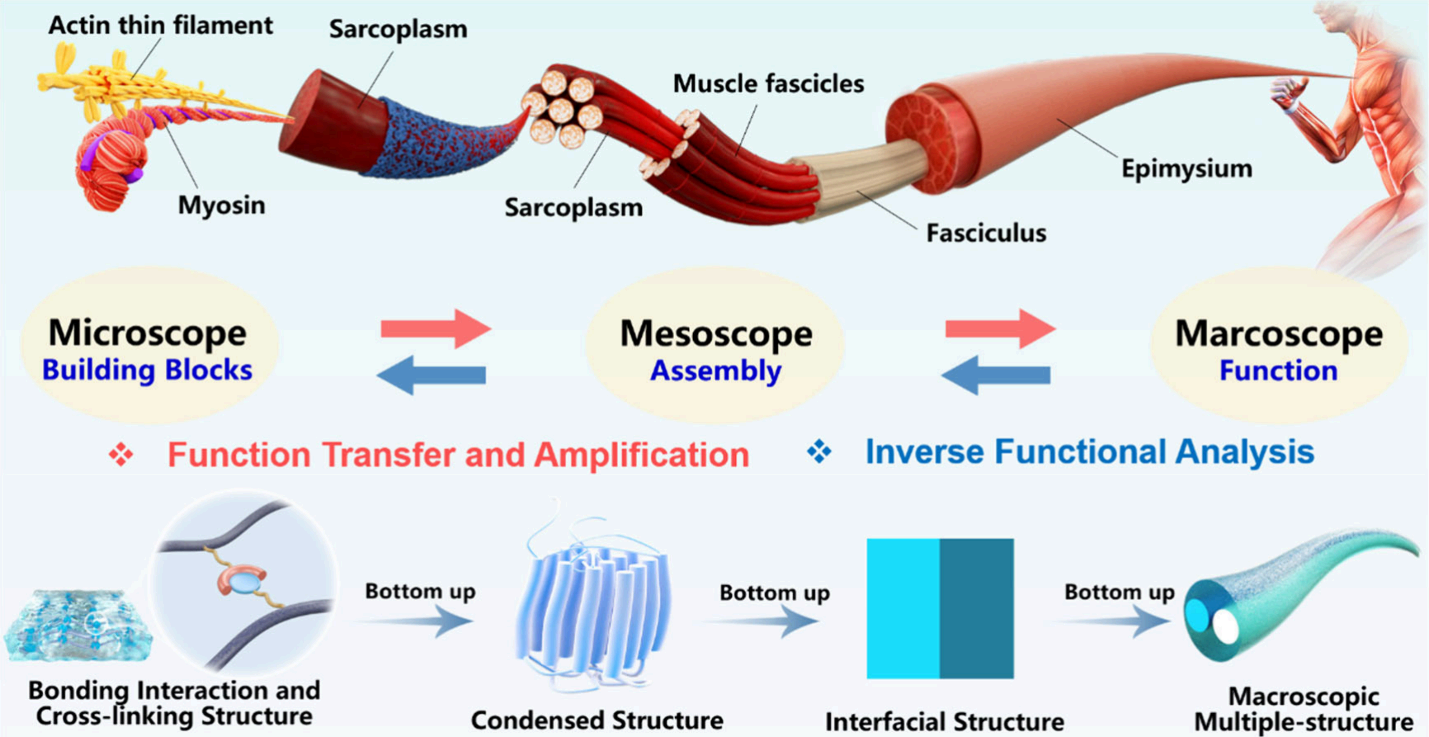
图4:以肌肉组织为例,展示了HFs从微观、介观到宏观的多尺度结构设计策略,并说明了不同层级结构对纤维性能的贡献
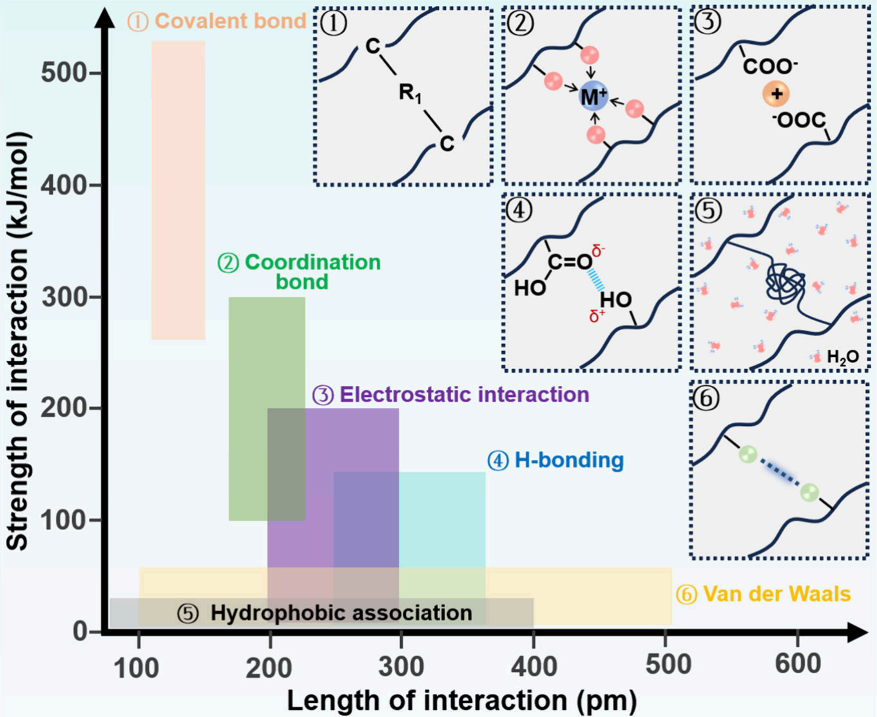
图5:总结了HFs中不同交联方式(共价键、配位键、静电作用、氢键、疏水相互作用、主客体作用)的键能、键长及其在微观结构调控中的应用
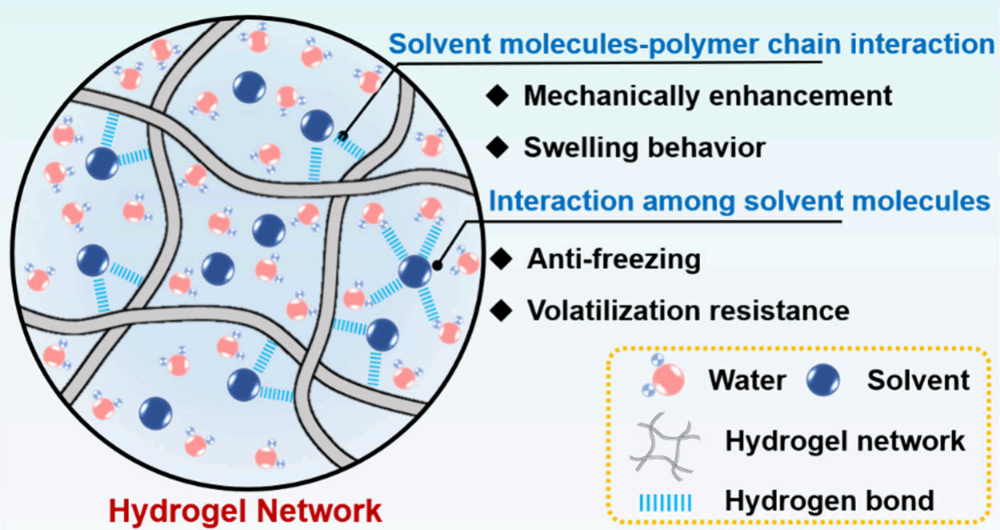
图6:展示了通过调控溶剂相(如水/有机溶剂比例、离子液体引入)来提升HFs耐低温、抗蒸发等性能的策略,并对其分子间作用机制进行了说明
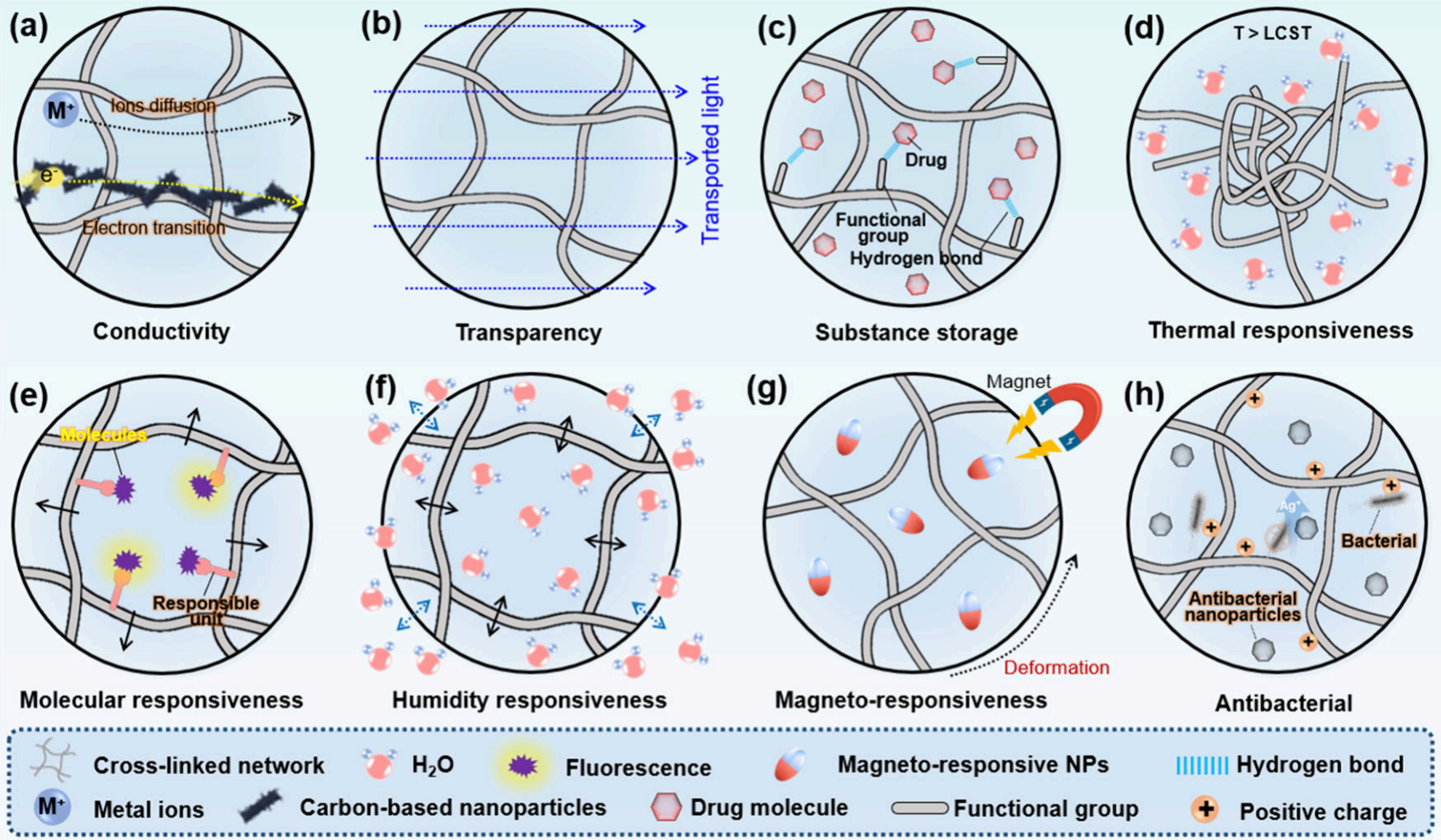
图7:系统总结了HFs功能相设计的主要方向,包括电导性、光透明性、药物释放、温度感应、分子识别、湿度响应、磁响应及抗菌性能
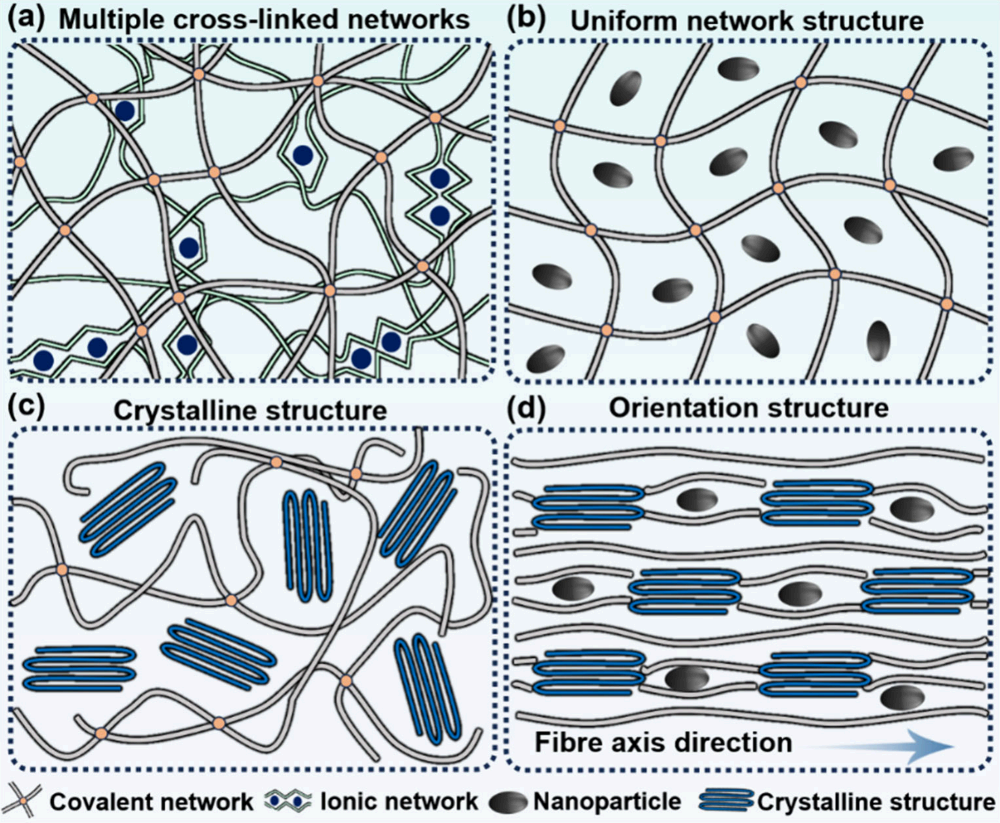
图8:说明了聚合物链的有序结晶及无定形区对HFs力学性能(如强度、延展性)的影响,强调通过结晶调控实现性能优化
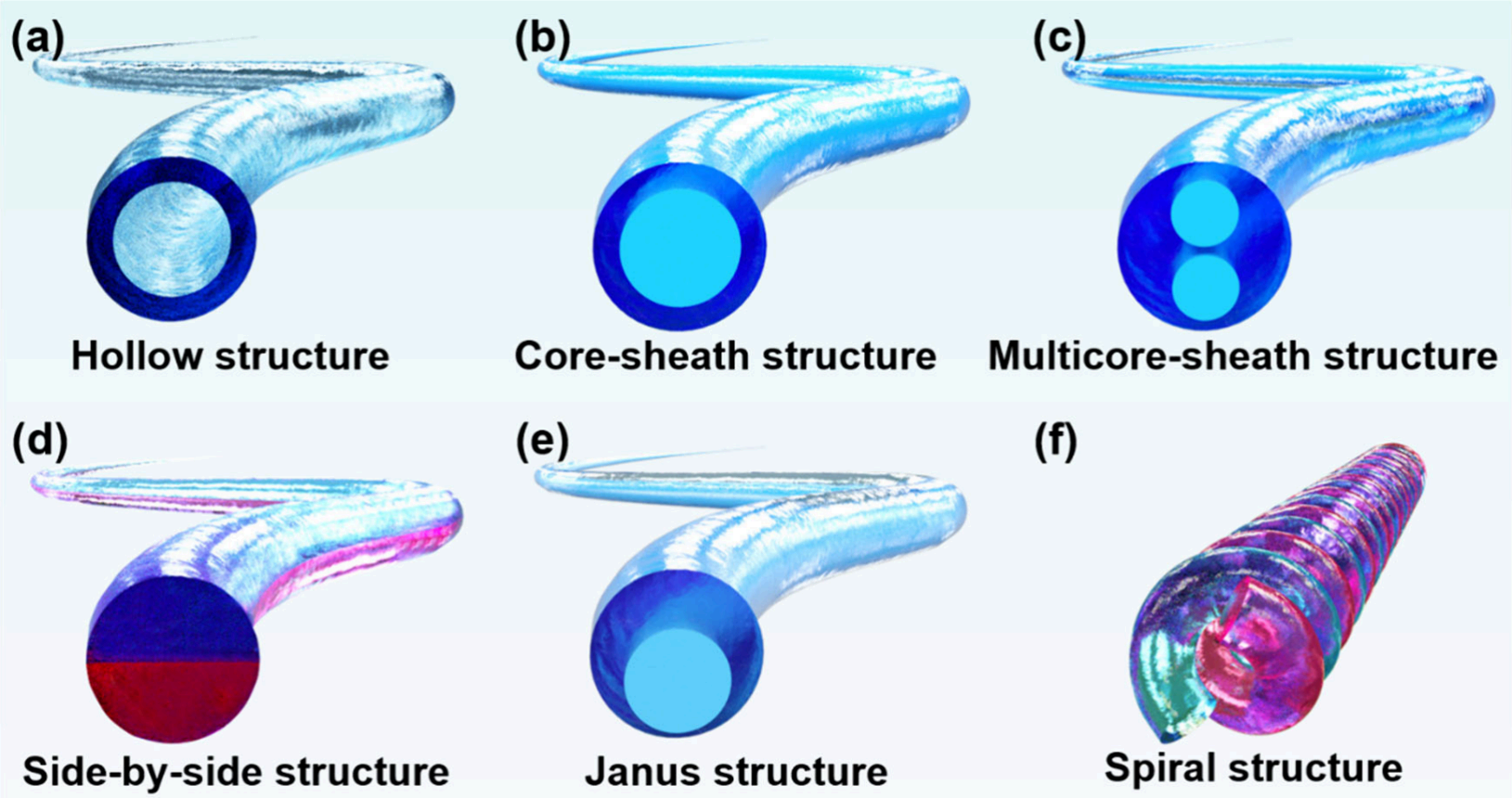
图9:罗列了不同导电填料(如碳纳米管、还原氧化石墨烯、银纳米线等)在HFs中的应用,及其对纤维导电性能的贡献
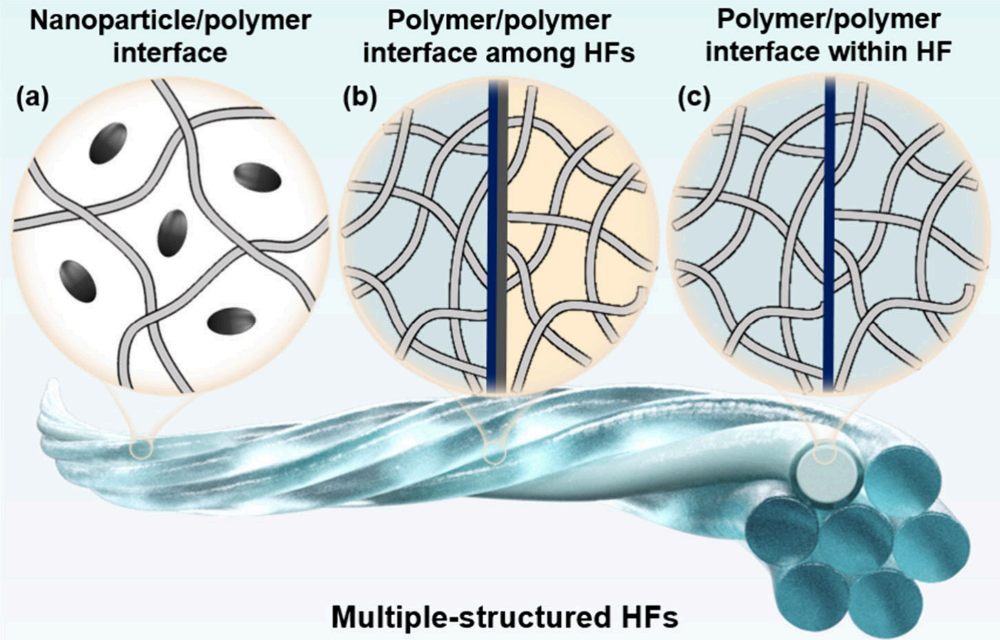
图10:总结了HFs凝胶化的四种机制:溶剂挥发诱导、溶剂状态诱导、扩散驱动物理/化学交联、聚合反应主导,并讨论了它们对纤维成形的作用
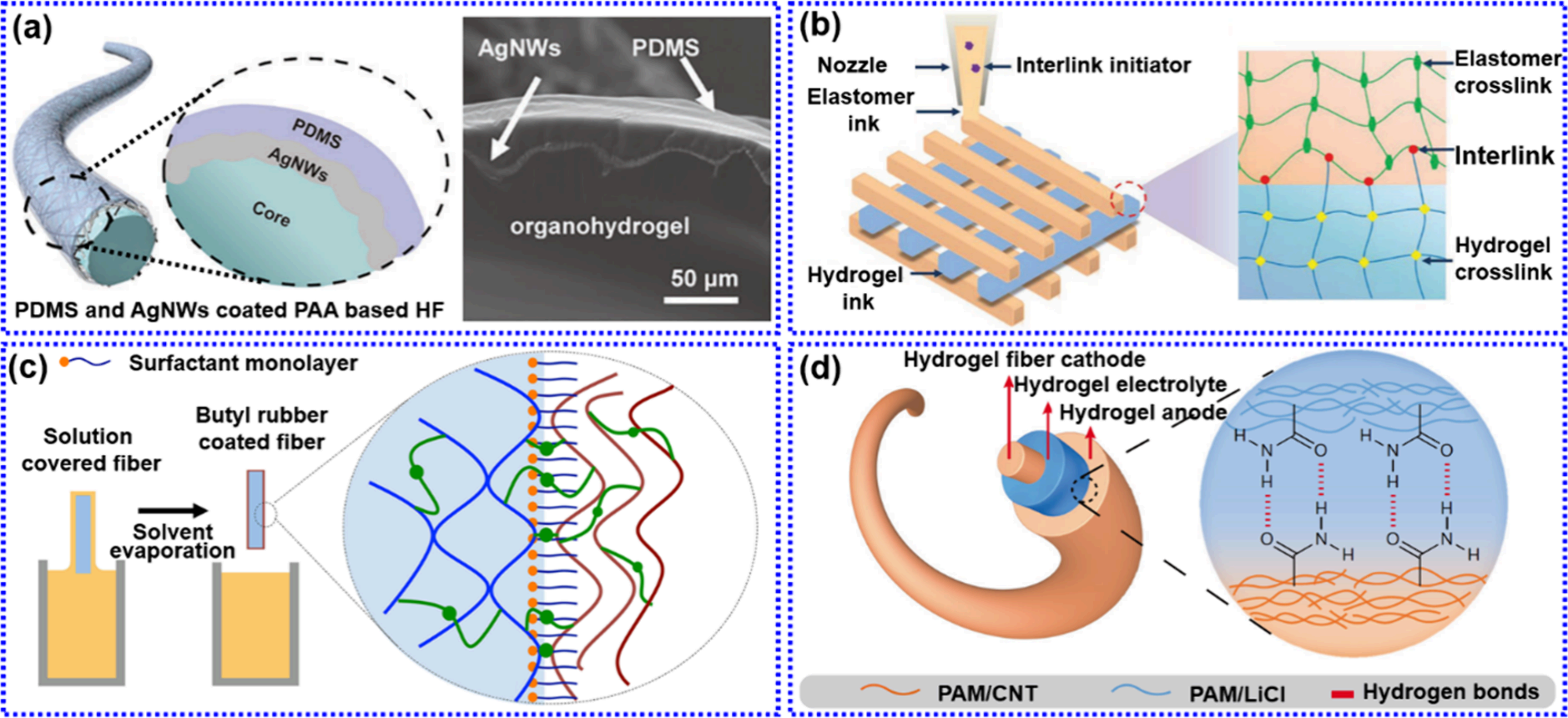
图11:展示了“纺丝前凝胶化”工艺流程,包括纺丝液制备、剪切流动成形及后续凝胶化过程,对纤维结构稳定性进行了强调
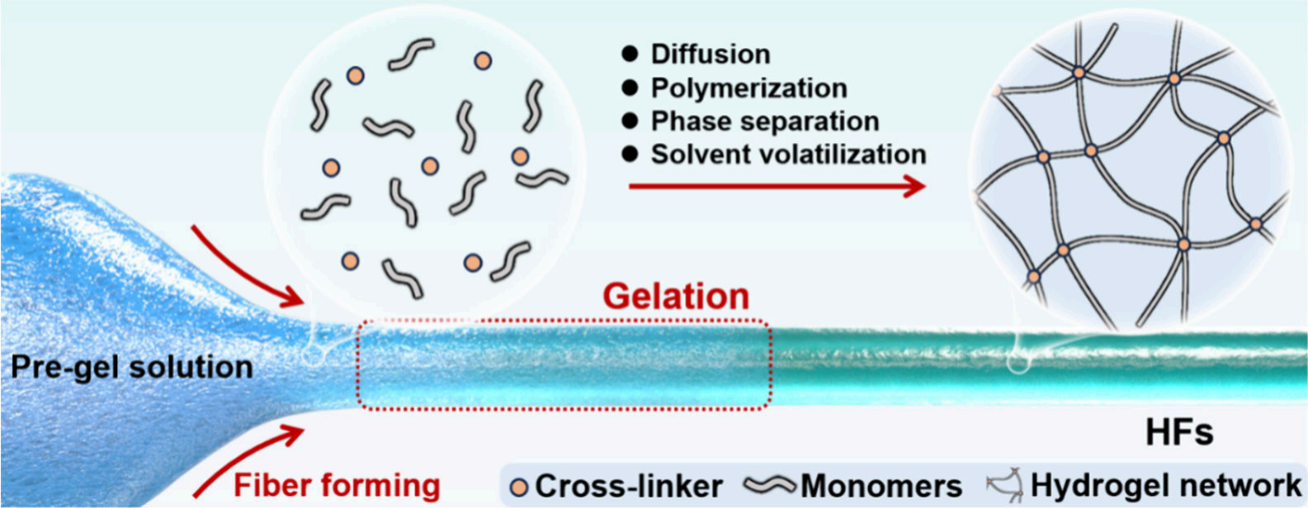
图12:说明了“纺丝后凝胶化”工艺,包括后浸泡交联、紫外光固化等,突出改善纤维形貌和提高网络完整性的效果
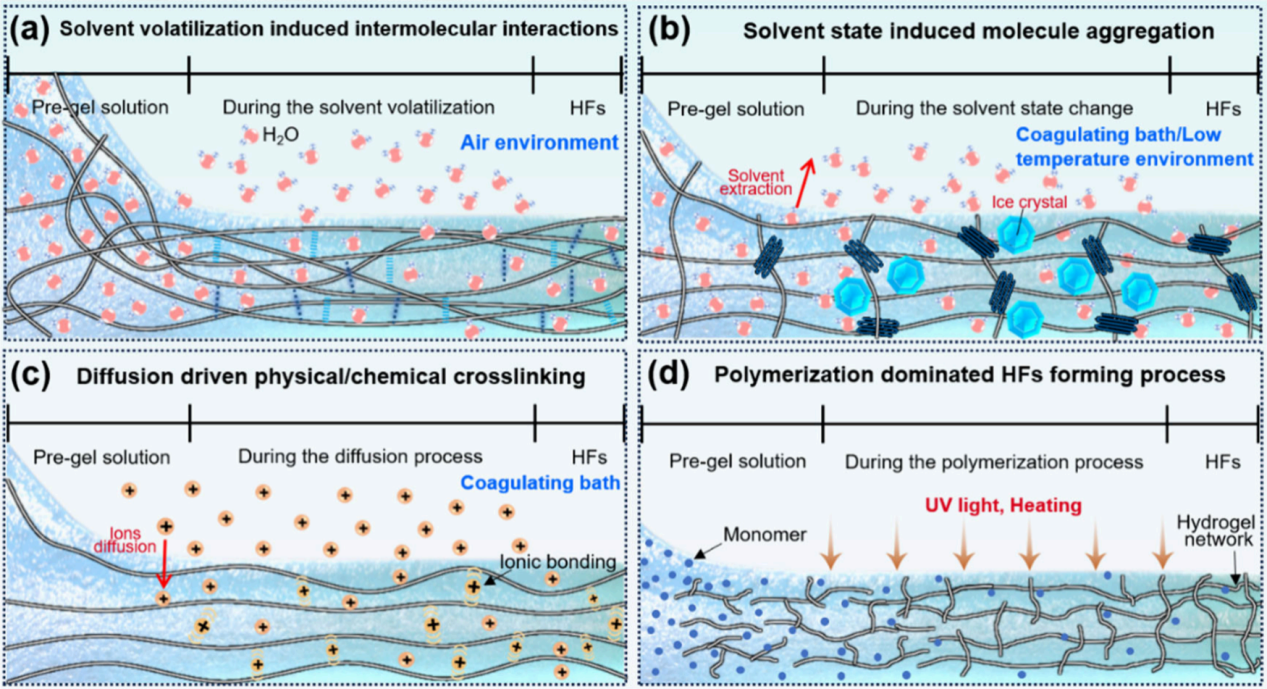
图13:概述了“纺丝过程中凝胶化”方法,强调了热诱导聚合、原位化学交联等在提高纤维连续性、致密性方面的应用优势
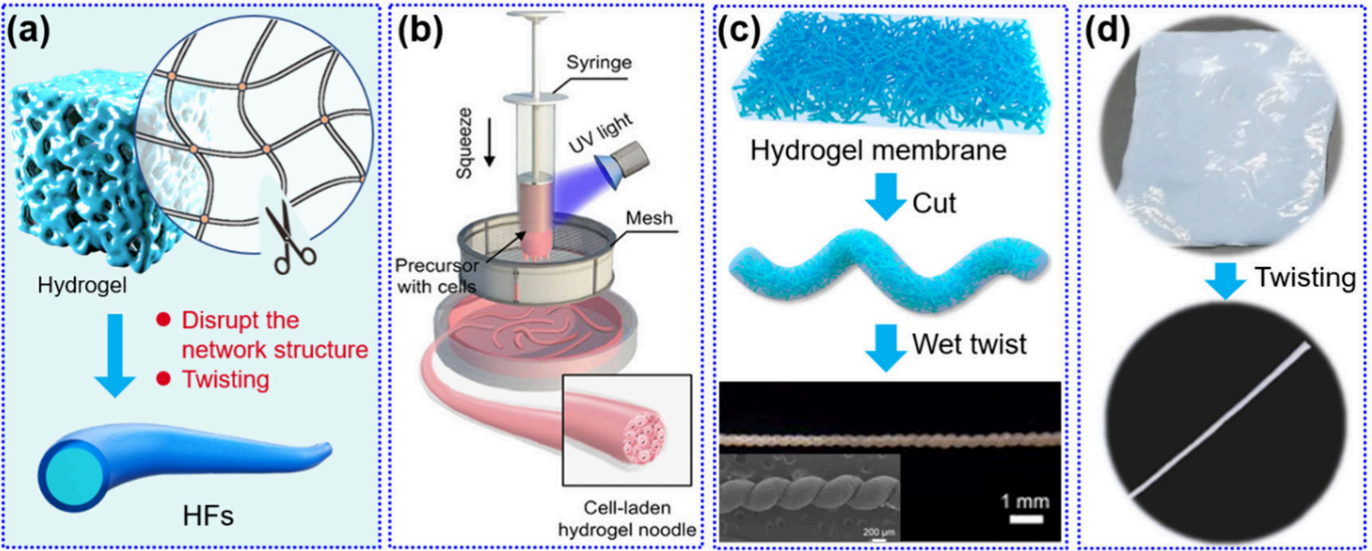
图14:展示了3D打印制备HFs的方法,包括熔融挤出打印与数字光处理技术,指出前体溶液黏弹性对纤维成形与精度的影响
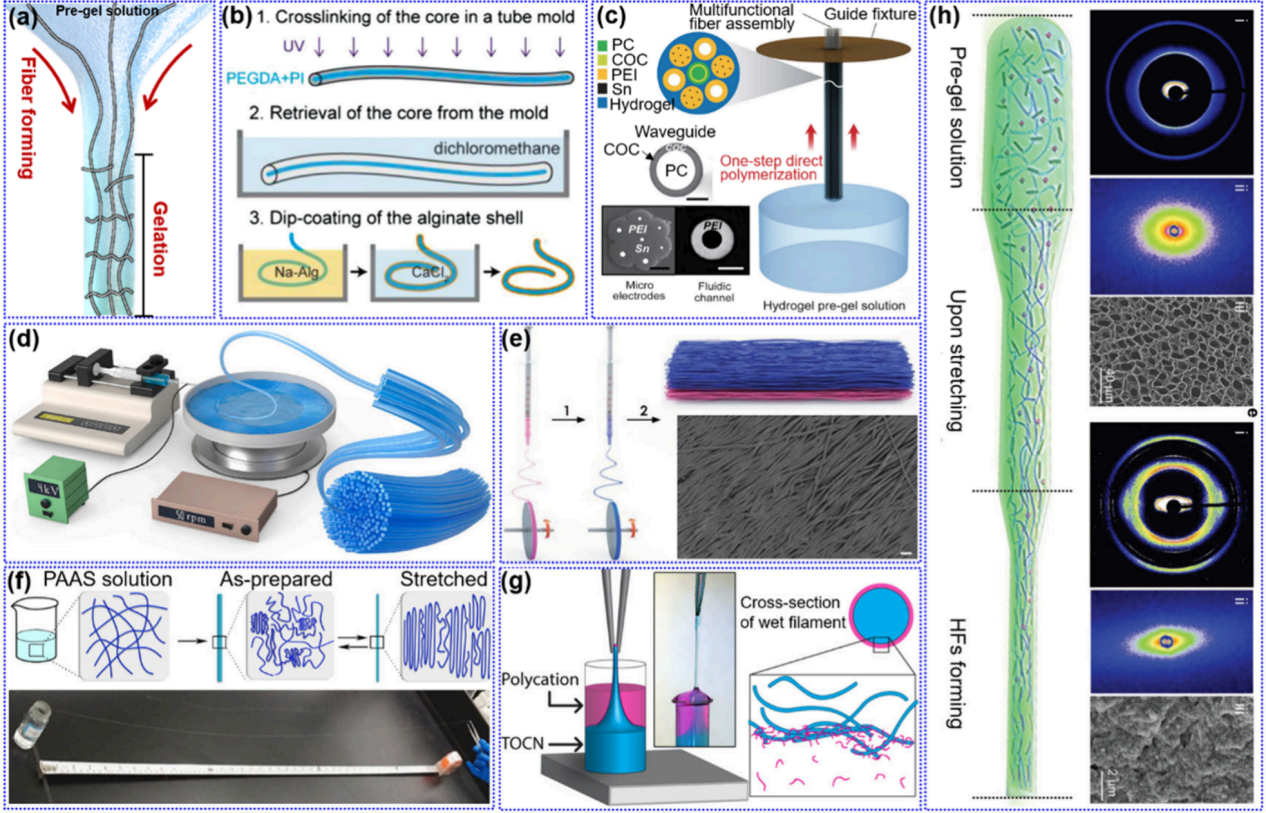
图15:介绍了微流控纺丝制备HFs的典型工艺流程,详细描述了液相交汇、紫外诱导聚合及离子交联机制

图16:总结了大规模HFs制备技术,包括湿纺、流延及连续反应纺丝,突出其在实现工业化、长尺度生产中的应用潜力
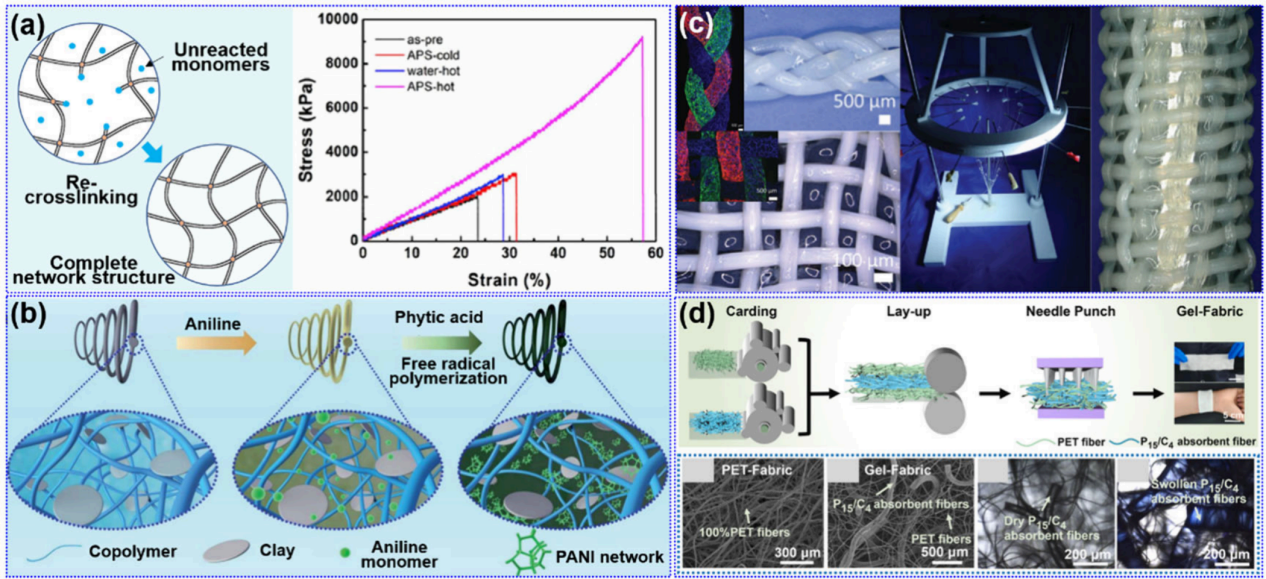
图17:阐述了HFs后处理工艺,如再交联、功能化修饰及纺织加工,并指出这些步骤在提升HFs力学与功能多样性方面的关键作用
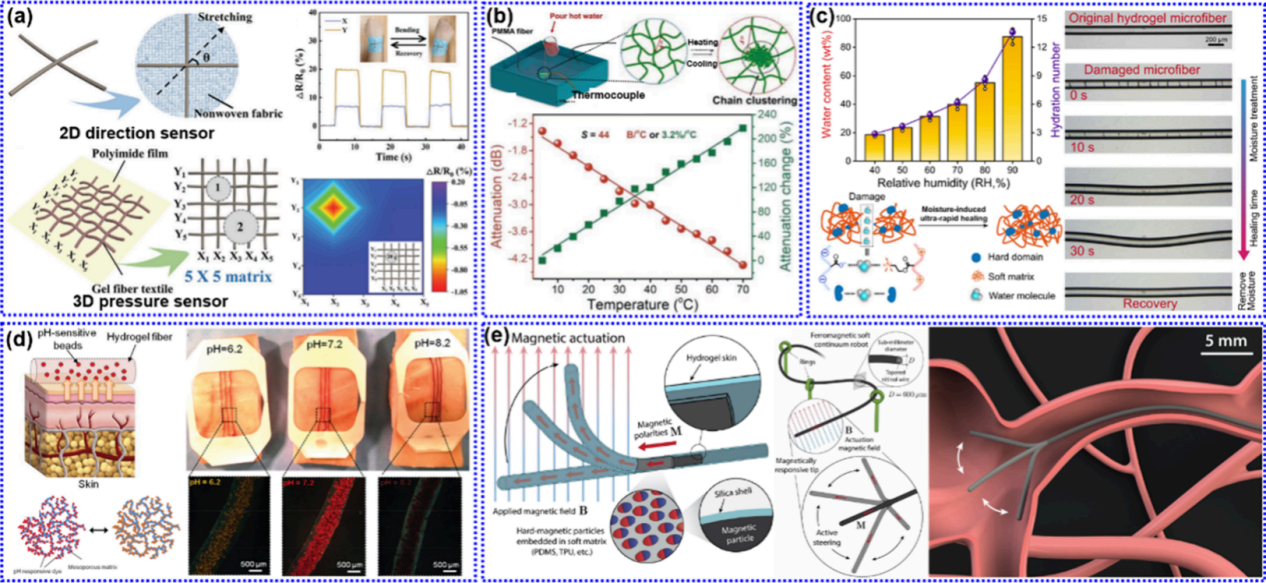
图18:展示了HFs在柔性传感器与驱动器中的应用,包括应变传感、温湿度感应、pH响应与磁响应软体机器人等
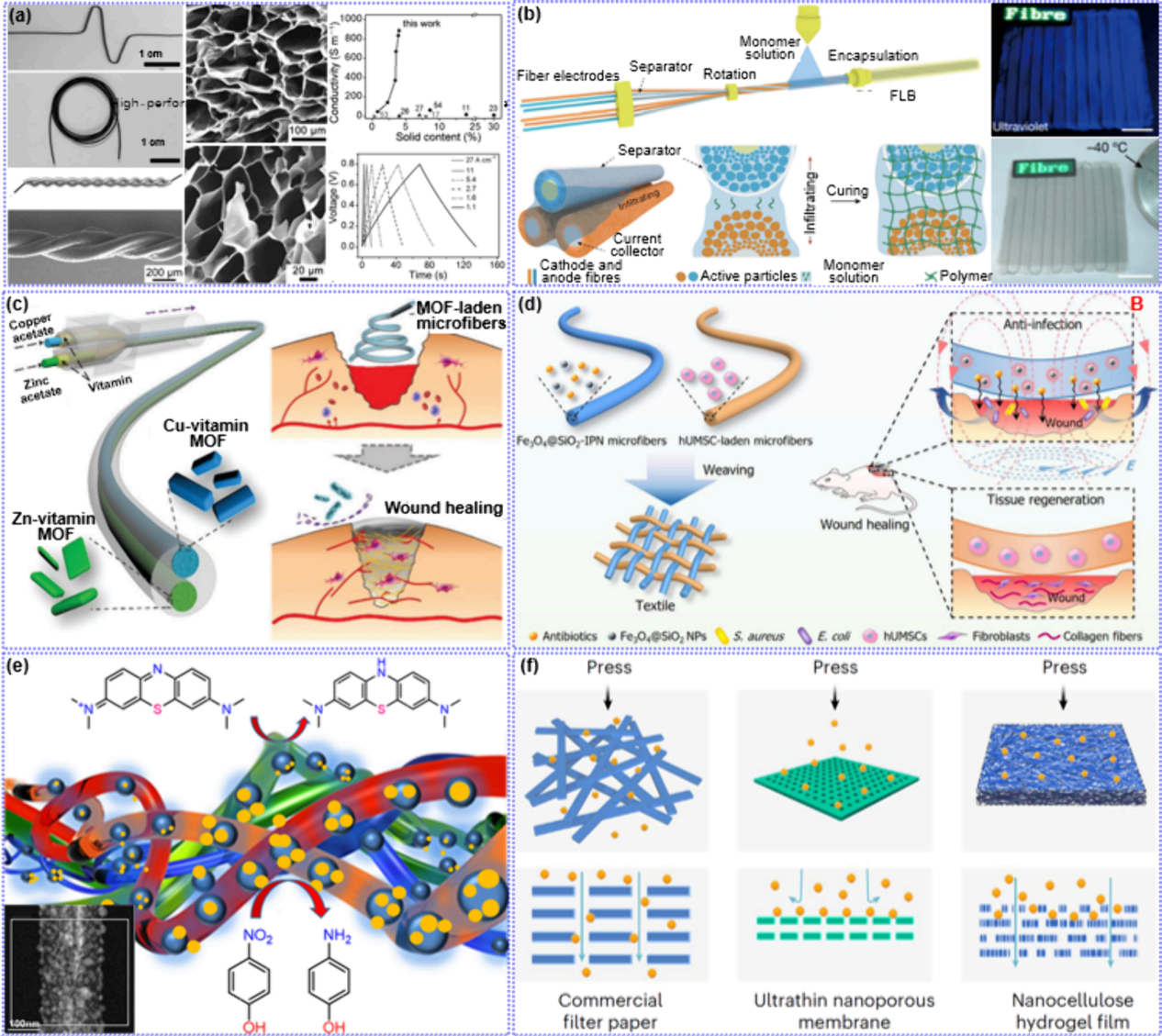
图19:概述了HFs在储能与物质传输(如电容器、药物缓释、水处理膜)中的应用,强调其高孔隙率对物质交换的促进作用
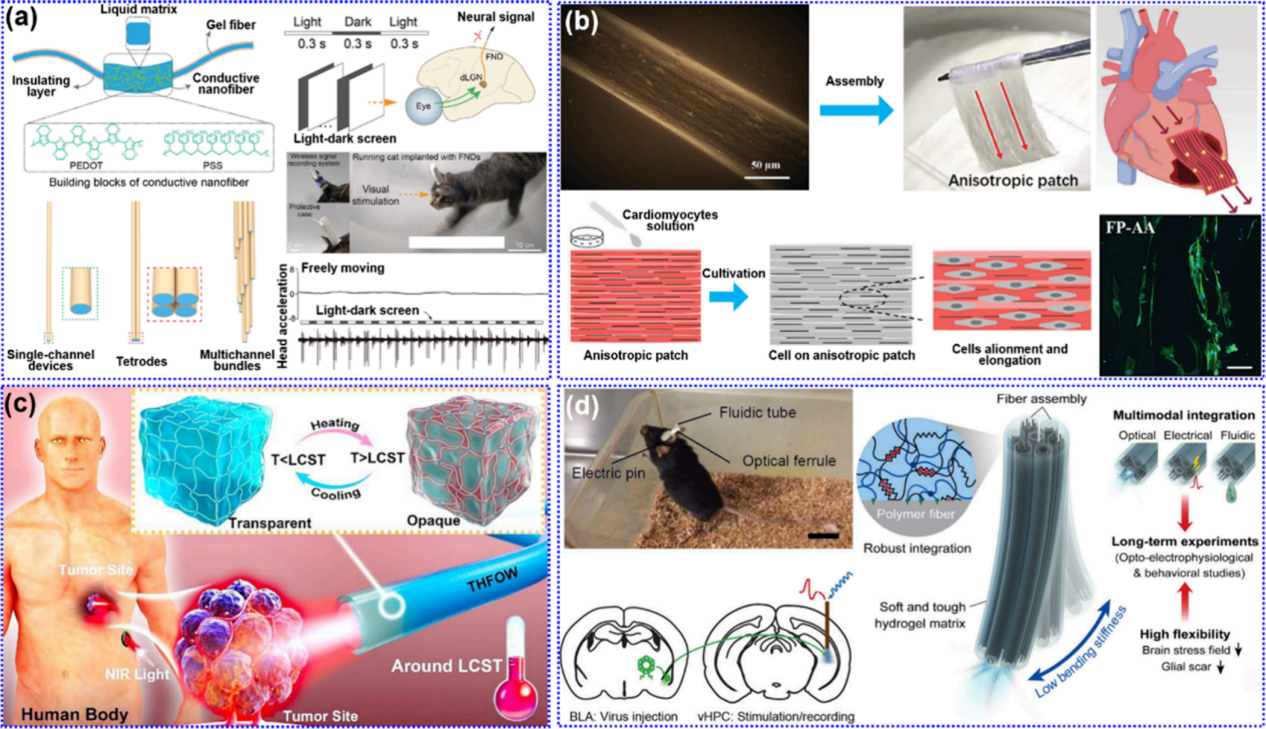
图20:总结了HFs在医疗电子与光子医学中的应用,如光子传输神经探针、深部组织治疗与生物光电子器件,突出了其低侵入性与良好生物相容性

图21:展示了HFs在组织工程(如骨、软骨、神经、皮肤)中的应用,强调其良好的细胞相容性、可降解性及对组织修复的支持功能
本综述系统梳理了水凝胶纤维从材料、结构、制备、性能到应用的全链条,尤其对静电纺丝、微流控纺丝、3D打印等成纤技术进行了重点讨论,对高校科研工作者、企业研发人员及产业应用团队均具有重要指导意义。
对于静电纺丝领域的研发人员,建议关注以下方向:
(1)采用多交联策略(如双网络、氢键+金属配位)提升HFs强度与疲劳寿命;
(2)开发原位静电纺丝+光交联技术,实现纤维成型与功能化同步进行;
(3)跨界拓展至生物电子器件、柔性能源器件;
(4)结合天然高分子(海藻酸、明胶)与功能纳米填料(如CNT、Ag NW)提升导电性与环境适应性;
(5)在产品设计中兼顾可降解性、生物相容性及长期使用稳定性。
此外,面向产业化生产,须解决:大规模连续生产技术;功能均匀性与结构一致性控制;器件封装与环境适应问题。
文章来源:https://doi.org/10.1021/acs.chemrev.5c00159

联系客服二维码

纳米纤维及其应用