联系我们
- 电话/微信:18520902353
- 客服QQ:3597831168
- 邮箱:info@wemaxnano.com
- 地址:广东省佛山市南海区狮山镇长兴西路12号建发风梅岭产业园9号楼

在微纳制造技术发展的推动下,静电纺丝技术凭借其独特优势,成为制备多功能纤维伤口敷料的重要手段。但现有静电纺丝伤口敷料多为二维结构,无法模拟天然细胞外基质的三维架构,限制了其应用,亟待创新改进 。近日,四川大学高分子科学与工程学院的徐家壮教授和李忠明教授团队在《Small》期刊发表了题为《Multifunctional Electrospun Fiber Sponge for Hemostasis and Infected Wound Healing》的最新研究成果。该团队通过结合湿度控制静电纺丝与冷冻干燥技术,成功开发出一种用于慢性伤口愈合的多功能静电纺纤维海绵(EFS)。该 EFS 凭借其独特的蓬松结构,展现出优异的吸水性、止血性、抗菌性和抗氧化能力。这一成果为创新性 3D 伤口敷料的工程设计提供了可行路径,极大地推动了感染伤口管理领域的进步,有望成为治疗感染伤口的有力候选方案。
团队在制备过程中,首先将聚乳酸(PLA)溶解在二氯甲烷(DCM)和N,N-二甲基甲酰胺(DMF)的混合溶剂中,制备成12 wt.%的PLA溶液。然后,利用湿度控制静电纺丝技术,设置相对湿度为90%,通过静电纺丝将PLA溶液制成纤维。在纺丝过程中,高湿度大气使聚乳酸(PLA)溶液发生湿度诱导相分离,使带电射流沉积成卷曲状,进而堆叠形成独特蓬松结构。最后,将收集到的纤维进行冷冻干燥,以去除残留溶剂并进一步固定纤维的海绵状结构。具体制备过程见图1。
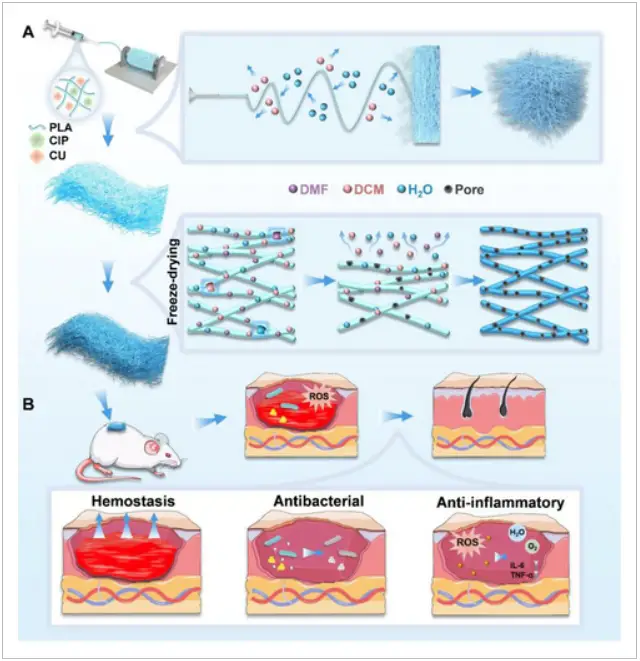
在制备过程中,团队发现通过调节工艺参数能够显著提升材料的性能。例如,将用于溶解聚乳酸(PLA)的二氯甲烷(DCM)和N,N-二甲基甲酰胺(DMF)混合溶剂比例调整为7:3,并将相对湿度控制在90%,由此制备得到的静电纺纤维海绵(EFS)展现出了极为优异的物理性能。经测试,该EFS的孔隙率高达99.8%,体积密度仅为2.8 mg/cm³,这使得其吸水率表现极为突出,能够吸收自身重量约5.39倍的水分(见图2e-f)。此外,在经历100次压缩循环测试后,EFS的压缩回弹性依然能够达到87.9%,这充分证明了其具备良好的形状稳定性,能够在实际应用中保持结构完整,有效发挥其功能特性。
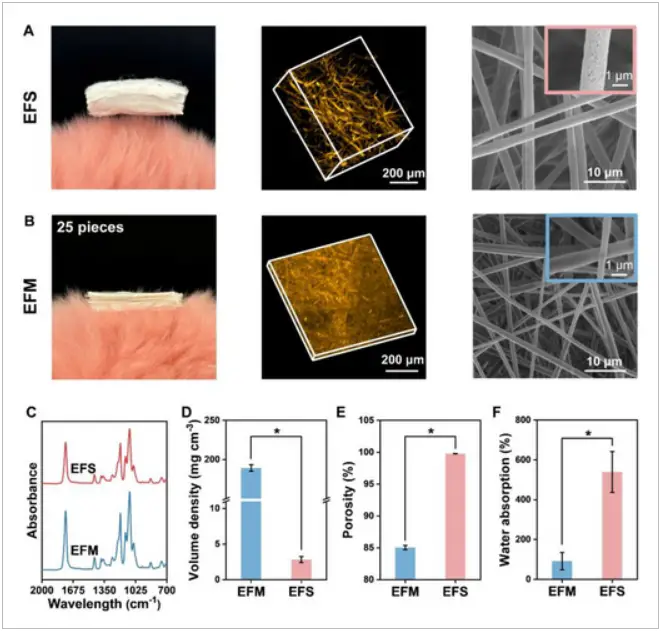
图2. EFS 的形态和结构。A) EFS 和 B) EFM 的共聚焦激光扫描显微镜 (CLSM) 及扫描电子显微镜 (SEM) 图像。C) 傅里叶变换红外光谱 (FTIR)。D) 体积密度。E) 孔隙率。F) 吸水率。每组 n = 3;* 表示 p < 0.05。
团队进一步对EFS进行功能化改性,通过在PLA纺丝溶液中掺入药物姜黄素(CU)和盐酸环丙沙星(CIP),制备得到具有抗菌和抗氧化功能的复合纤维海绵(命名为CC@EFS)。实验结果显示,与传统的二维纤维膜(CC@EFM)相比,CC@EFS在体外实验中展现出更显著的药物释放效果,在相同时间内累积释放的CU量远大于CC@EFM(见图3a)。这主要归功于CC@EFS的高孔隙率为药物释放提供了充足的交换空间。在抗菌性能测试中,CC@EFS对金黄色葡萄球菌(S. aureus)的抑制圈直径约为CC@EFM的10倍,并且对大肠杆菌(E. coli)和金黄色葡萄球菌的抗菌率分别达到99.7%和97.8%,显著高于CC@EFM(见图3b、d)。此外,CC@EFS对DPPH自由基的清除率达到92.9%,也远高于CC@EFM,表明其具有更强的抗氧化能力(见图3f)。
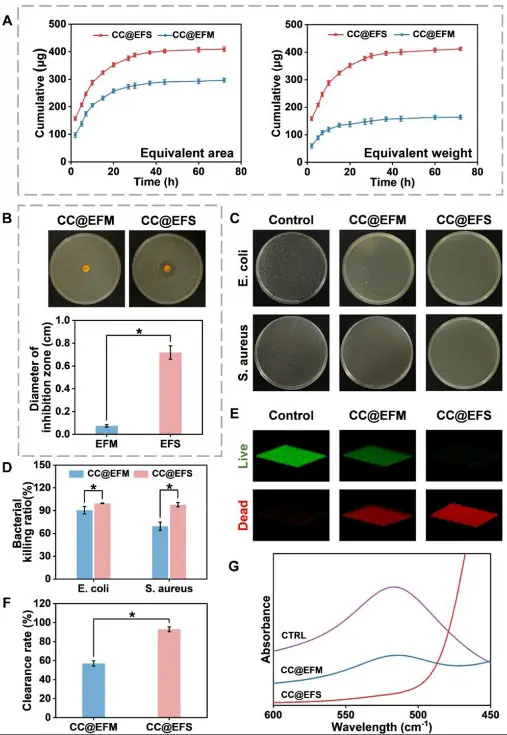
得益于其独特的蓬松形态,无论是体外实验还是体内实验,EFS及其药物复合版CC@EFS均展现出了优异的止血效果。在体外实验中,EFS和CC@EFS的血红蛋白捕获率超过20%,而传统的二维纤维膜(EFM)及其药物复合版(CC@EFM)的捕获率则不到13%。而在大鼠尾部截肢模型的体内止血评估中,CC@EFS组的血液损失量显著减少,进一步证实了其卓越的止血性能(见图4c-f)。
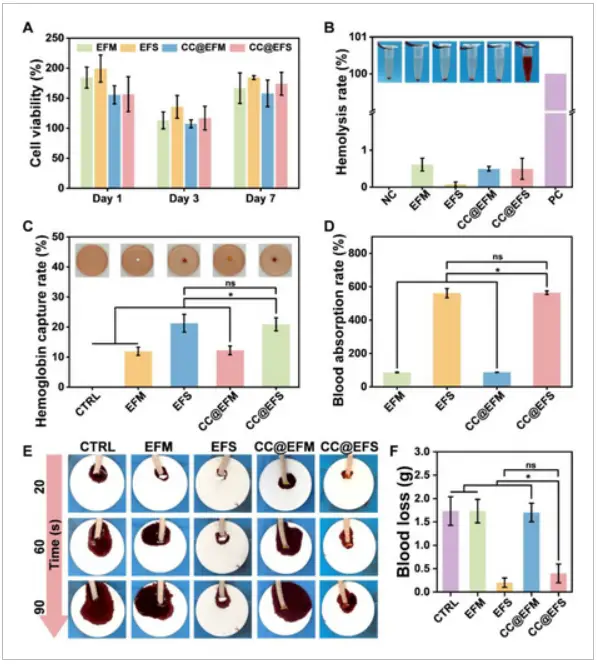
图4. CC@EFS 的体外生物相容性和止血性能。A) L929 细胞与样品提取物共培养 1 天后的 MTT 测试结果。B) 溶血率及相应图像。C) 血红蛋白捕获率及相应图像。D) 血液吸收率。E) 大鼠尾部截肢模型中样品的止血能力的连续图像。F) 血液损失量的统计分析。每组 n = 3;* 表示 p < 0.05;ns 表示无显著差异。
在体内感染伤口愈合评估实验中,团队利用S. aureus感染的全层大鼠伤口模型对CC@EFS进行了全面测试。结果显示,CC@EFS组的伤口在第3天就明显恢复,第14天几乎完全再上皮化。组织学评估进一步揭示了CC@EFS的卓越性能:其伤口宽度最小,肉芽组织生长最快且厚度最大,并且在第14天形成了更成熟的毛囊。免疫荧光染色分析表明,CC@EFS组在第7天显著抑制了促炎细胞因子TNF-α和IL-6的表达,有效缩短了炎症期;而在第14天则表现出最强的血管生成标志物CD31和VEGF的表达,表明其能够有效促进血管再生(见图5)。这些发现充分证实了CC@EFS在消除病原菌、抑制炎症反应以及促进伤口愈合方面的显著优势。
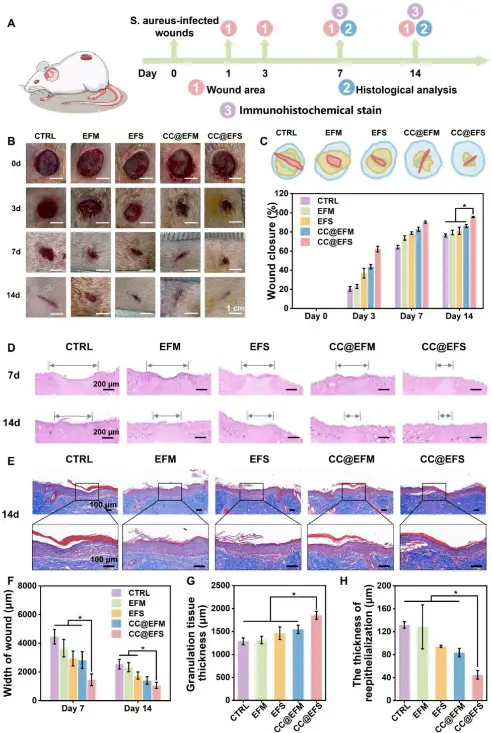
图5. 体内伤口再生评估。A) 动物实验的时间表。B) 伤口进展的代表性图像,以及 C) 第 0、3、7 和 14 天的伤口闭合数据的追踪分析和定量结果。D) 第 7 天和第 14 天的 H&E 染色。E) 第 14 天的 Masson 三色染色及局部放大图。F) 伤口宽度。G) 肉芽组织厚度。H) 再上皮化厚度。每组 n = 3;* 表示 p < 0.05。
在本研究中,团队开发了一种简便且可扩展的策略,通过将湿度控制静电纺丝与冷冻干燥固化相结合来制备多功能静电纺丝纤维海绵(EFS)。优化工艺参数后的海绵具有优异的吸水率和形状稳定性。通过掺入 CU 和 CIP,所得的 CC@EFS 表现出卓越的抗菌和清除 ROS 的能力。此外,独特的蓬松形态在体外和体内均增强了止血效果。本研究为制备海绵敷料提供了一种新颖且高效的策略,在对抗伤口感染和加速伤口愈合方面具有巨大的潜力。
文章来源:https://doi.org/10.1002/smll.202409969

联系客服二维码

纳米纤维及其应用